 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
试为下述反应设计一电池 Cd(s)+I2(s)====Cd2+()+2I-() 求电池在298K时的标准电动势、反应的和平衡常数。如
试为下述反应设计一电池
Cd(s)+I2(s)====Cd2+(a=1)+2I-(a=1)
求电池在298K时的标准电动势E、反应的△rG和平衡常数Kθ。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
试为下述反应设计一电池
Cd(s)+I2(s)====Cd2+(a=1)+2I-(a=1)
求电池在298K时的标准电动势E、反应的△rG和平衡常数Kθ。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“试为下述反应设计一电池 Cd(s)+I2(s)====Cd2…”相关的问题
更多“试为下述反应设计一电池 Cd(s)+I2(s)====Cd2…”相关的问题
298K时,有反应Pb(s)+Cu2+(a=0.5)→Pb2+(a=0.1)+Cu(s),试为该反应设计电池,并计算:
(1)电池电动势;
(2)电池反应的Gibbs能变化;
(3)若将上述反应写成2Pb(s)+2Cu2+(a=0.5)→2Pb2+(a=0.1)+2Cu(s),(1)、(2)所得结果有何变化?
298K时,有反应Pb(S)+Cu2+(a=0.5)→Pb2+(a=0.1)+Cu(s),试为该反应设计电池,并计算:(1)电池电动势;(2)电池反应的Gibbs能变化;(3)若将上述反应写成2Pb(S)+2Cu2+(a=0.5)→2Pb2+(a=0.1)+2Cu(S),(1)、(2)所得结果有何变化?
反应I2(s)+Cl2(g)====2ICl(g)

(A) 14.7kJ·mol-1; (B) 1.18kJ·mol-1;
(C) 3.2kJ·mol-1; (D) -4.7kJ·mol-1。
CSTR的稳定操作状态
在一全混流反应釜中进行下述一级不可逆液相反应:
k1=1.8×106exp(-6039.25/T),反应混合物的密度ρ和比热cp,均为常数,ρ=1.2g/cm3,cP=3.768J/(g·K)。在20℃液料以200cm3/s的速度进入反应釜。原料中只含反应物A,其初浓度为4mol/L。反应釜的体积为10L。反应在绝热条件下进行。已知该反应的热效应为△Hr=-192.95kJ/mol。试确定该反应体系的稳定工作点和相应的转化率。
测得电池Zn|ZnCl2(a=0.05)|AgCl(s)|Ag的电动势在298.15K时为1.015V,温度系数TCR为-4.92×10-4V/K,试写出电池反应并计算当电池可逆放电2mol电子电量时,电池反应的△rGm、△rSm、△rHm及电池的可逆热Qr。
在298K时,下述电池的电动势E=0.1519V:
Ag(s)|AgI(s)|HI(a=1)|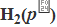 |Pt
|Pt
并已知下列物质的标准摩尔生成焓:
| 物 质 | AgI(s) | Ag+ | I- |
 | -62.38 | 105.89 | -55.94 |
试求:

298K时,已知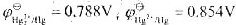 ,试计算(1)反应Hg2++e→1/2Hg22+的标准电极电势。(2)为反应Hg+Hg2+→Hg2-设计电池,并计算该反应的标准平衡常数。
,试计算(1)反应Hg2++e→1/2Hg22+的标准电极电势。(2)为反应Hg+Hg2+→Hg2-设计电池,并计算该反应的标准平衡常数。
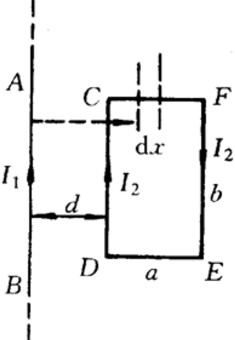
如图所示,无限长直导线AB内通有电流I1,与其共面的有一矩形线框CDEF,通有电流I2,CD、EF均平行于AB,CF长为a,EF长为b,AB与CD间距为d。
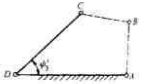
如图所示,现欲设计一铰链四杆机构,设已知摇杆CD的长lCD=75mm,行程速比系数K=1.5,机架AD的长度为lAD=100mm,摇杆的一个极限位置与机架间的夹角为 ,试求曲柄的长度lAB和连杆的长度lBC(有两组解)。
,试求曲柄的长度lAB和连杆的长度lBC(有两组解)。
当I2作为催化剂时,氯苯(C6H5Cl)与Cl2在CS2(1)溶液中发生如下的平行反应(均为二级反应):
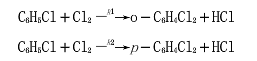
设在温度和I2的浓度一定时,C6H5Cl及Cl2在CS2(1)溶液中的起始浓度均为0.5mol·dm-3,30min后有15%的C6H5Cl转变为o-C6H4Cl2,有25%的C6H5Cl转变为p-C6H4Cl2,试计算两个速率常数k1和k2。
根据下列反应,判断氧化性强弱顺序为()。①H2S+Cl2=S+2HCl,②2NaI+Cl2=2NaCl+I2③Na2S+I2=2NaI+S
A.Cl2>I2>S
B.Cl2>S>I2
C.I2>Cl2>S
D.S>I2>Cl2