 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
在300K时,1.0mol理想气体反抗100.0kPa恒外压,从1.0dm3</sup>膨胀列 10.0dm3</sup>,试计算此过程体系吸收的热量。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在300K时,1.0mol理想气体反抗100.0kPa恒外压…”相关的问题
更多“在300K时,1.0mol理想气体反抗100.0kPa恒外压…”相关的问题
A.向左进行
B.向右进行
C.处于平衡状态
D.无法确定
已知反应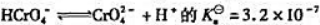 反应
反应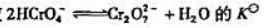 =33.
=33.
(1)计算反应 的标准平衡常数Kθ;
的标准平衡常数Kθ;
(2)计算1.0mol·L-1K2CrO4溶液中CrO42-与Cr2O72-浓度相等时溶液的pH.
已知气体l2相邻振动能级的能量差Δɛ=0.426X10-20J;试求300K时1分子的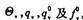 .
.
已知某反应的活化能为70kJ·mol-1,300K时的速率常数为0.1s-1,试计算
(1)400K时,反应的速率为原来的多少倍?
(2)温度由1000K升高到1100K时,反应速率为1000K时的多少倍?
已知300时,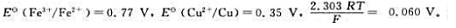 则可逆反应:
则可逆反应: 在300K时的标准平衡常数为()
在300K时的标准平衡常数为()
A、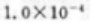
B、
C、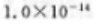
D、
p2=50kPa.已知固态物质A的Cp,m=24.454J·mol-1·K-1.试求:
(1)系统的末态温度T2;
(2)以B为系统时,过程的W,Q,ΔU和ΔH.
A.>1;
B.<1;
C.=1;
D.无法判断