 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在恒温恒容条件下可逆反应N2(g)+3H2(g)===2NH3(g),下列能够说明反应已经达到平衡状态的是()
A.(N2)∶c(H2)∶c(NH3)=1∶3∶2
B.氨气的百分含量不再变化
C.断开1个N≡N键的同时有6个N—H键生成
D.混合气体的质量不随时间的变化而变化
 答案
答案
B、氨气的百分含量不再变化
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.(N2)∶c(H2)∶c(NH3)=1∶3∶2
B.氨气的百分含量不再变化
C.断开1个N≡N键的同时有6个N—H键生成
D.混合气体的质量不随时间的变化而变化
 答案
答案
B、氨气的百分含量不再变化
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在恒温恒容条件下可逆反应N2(g)+3H2(g)===2NH…”相关的问题
更多“在恒温恒容条件下可逆反应N2(g)+3H2(g)===2NH…”相关的问题
A.气体总质量不变
B.混合气体密度不变
C.反应物B的浓度不变
D.混合气体平均相对分子质量不再改变
A.10s
B.大于10s
C.小于10s
D.无法判断
偶氮甲烷(CH3NNCH3)气体的分解反应
(CH3NNCH3)(g)→C2H6(g)+N2(g).
为一级反应.在287℃的真空密闭恒容容器中充入初始压力为21.332kPa的偶氮甲烷气体,反应进行1000s时测得系统的总压为22.732kPa,求速率常数k及半衰期t1/2.
A.偏摩尔量是在恒温恒容条件下,广延量对摩尔数的偏微商
B.偏摩尔量的意义是恒温恒压下向无限大的体系中加入一摩尔组分后体系某性质的变化
C.恒温恒压下向有限的体系中加入足够小的dni摩尔的组分所引起的体系性质变化dXi,则dXi与dni之比值就是偏摩尔量
D.离子熵就是水溶液中离子的偏摩尔熵
已知某恒温恒容反应的机理如下:
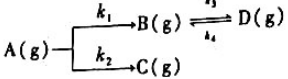
反应开始时只有A(g),且已知CA.o=2.0mol·dm-3,k=3.0s-1,kz=2.5s-1,k3=4.0s-1,k4=5.0s-1.
(1)试写出分别用cA,CB,Cc,CD表示的速率方程;
(2)求反应物A的半衰期;
(3)当反应物A完全反应(即cA=0)时,CB,Cc,CD各为多少?
已知氮(N2,g)的摩尔定压热容与温度的两数关系为
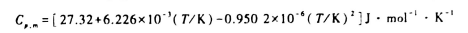
将始态为300K,100kPa下的1molN2(g)置于1000K的热源中,求系统分别经(1)恒压过程;(2)恒容过程达到平衡态时的Q,ΔS及ΔSm.