 更多“铜锌原电池工作时,电子经电解质溶液从锌电极流向铜电极()”相关的问题
更多“铜锌原电池工作时,电子经电解质溶液从锌电极流向铜电极()”相关的问题
A.将反应2Fe3++Fe===3Fe2+设计为原电池,则可用Zn为负极,Fe为正极,FeCl3为电解质
B.铜片和铝片用导线连接后插入浓硝酸中,铜作负极
C.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
D.铝片和镁片用导线连接后插入NaOH溶液中,Mg较活泼作负极
A.手机上用的锂离子电池属于二次电池
B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
C.氢氧燃料电池可把化学能转化为电能
D.锌锰干电池中,锌电极是负极
A.14 g乙烯和丙烯混合物中含原子数目为2NA
B.50 g KHCO3和CaCO3混合物含离子数目为2NA
C.23 g Na与O2完全反应生成Na2O和Na2O2的混合物,转移的电子数目为NA
D.铜—锌原电池(电解质溶液为稀硫酸)的电路中每转移2NA个电子,正极生成22.4 L H2
A.锌为正极,Ag2O为负极
B.原电池工作时,负极区PH增大
C.原电池工作时,负极区PH增大,正极区PH减小
D.锌为负极:Zn+2OH--2e- =ZnO+H2O
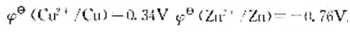 ,求此时原电池的电动势比标准状态时的电动势()
,求此时原电池的电动势比标准状态时的电动势()A.上升0.24V
B.下降0.24V
C.上升0.12V
D.下降0.12V
某化学小组的同学为探究原电池原理,设计如图所示装置,将锌、铜通过导线相连,置于稀硫酸中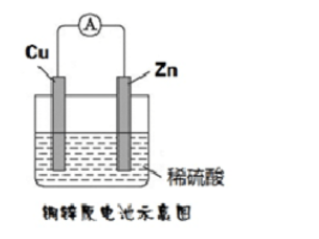 (1)外电路,电子从()极流出。溶液中,阳离子向()极移动。
(1)外电路,电子从()极流出。溶液中,阳离子向()极移动。
(2)若反应过程中有0.2mol电子发生转移,则生成的气体在标准状况下的体积为()。
(3)该小组同学将稀硫酸分别换成下列试剂,电流计仍会偏转的是()(填序号)。
A.无水乙醇
B.醋酸溶液
C.CuSo4溶液
D.苯
(4)实验后同学们经过充分讨论,认为符合某些要求的化学反应都可以通过原电池来实现。下列反应可以设计成原电池的是()(填字母代号)。
A.NaOH+HCl=NaCl+H2O
B.2H2+O2=2H2O
C.Fe+2FeCl3=3FeCl2
D.2H20=2H2↑+2O2↑
A.根据反应Cu+H2SO4=CuSO4+H2↑设计的原电池中铜作负极
B.钠块与铜用导线连接后插入到稀盐酸中发现铜的表面很快有大量的气泡冒出
C.根据原电池原理,可以将反应2H2+O2=2H2O设计成原电池,且H2在负极反应
D.构成闭合回路是形成原电池的必备要素之一,电子在此闭合回路中从负极流经导线到达正极,再从正极经电解质溶液流回负极


 如果结果不匹配,请
如果结果不匹配,请 

















