 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知某原电池的电池反应为Zn(s)+Cu2+(aq)→Zn2+(aq)+Cu(s),如果要提高该原电池的电动势,可增加( )
A.Zn2+浓度
B.Cu2+浓度
C.Zn(s)尺寸
D.Cu(s)尺寸
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.Zn2+浓度
B.Cu2+浓度
C.Zn(s)尺寸
D.Cu(s)尺寸
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知某原电池的电池反应为Zn(s)+Cu2+(aq)→Zn2…”相关的问题
更多“已知某原电池的电池反应为Zn(s)+Cu2+(aq)→Zn2…”相关的问题
A.(-)Zn(s)|CuSO4(c1)||ZnSO4(c2)|Cu(s)()
B.(-)ZnSO4(c1)|Zn(s)|"Cu(s)|CuSO4(c2)()
C.(-)Cu(s)||CuSO4(c1)|ZnSO4(c2)|Zn(s)()
D.(-)Zn(s)IZnSO4(c1)||CuSO4(c2)|Cu(s)()
A.正极反应为:Zn—2e-=Zn2+
B.在外电路中,电流从负极流向正极
C.电池反应为:Zn+Cu2+=Zn2++Cu
D.盐桥中的K+移向ZnSO4溶液
A.Zn、Cu、ZnSO4
B.u、Zn、 ZnCl2
C.u、Zn、CuCl2
D.Zn、Cu、CuSO4
A.①②
B.②③
C.③④
D.②④
A.无论a和b是否连接均可形成原电池
B.和b不连接时,铁片上会有金属铜析出
C.和b用导线连接时,铜片上发生的反应为Cu2++2e-= Cu
D.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色
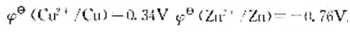 ,求此时原电池的电动势比标准状态时的电动势()
,求此时原电池的电动势比标准状态时的电动势()A.上升0.24V
B.下降0.24V
C.上升0.12V
D.下降0.12V
298K时,在Ag+/Ag电极中加入过量I-,设达到平衡时c(I-)=0.1mol·dm-3,而另一电极为Cu2+/Cu,c(Cu2+)=0.01mol·dm-3,将两电极组成原电池,写出原电池符号、电池反应,并求电池反应平衡常数。
已知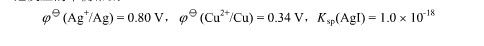
A.Sn2++2H+Sn4++H2
B.Sn4++H2Sn2++2H+
C.Sn4++2H+Sn2++H2
D.Sn2++H2Sn4++2H+
原电池是将化学能转变为电能的装置,关于如图所示原电池的说法正确的是()。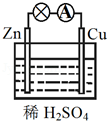
A.Cu为负极,Zn为正极
B.电子由铜片通过导线流向锌片
C.正极反应式为Zn﹣2e﹣=Zn2+
D.原电池的反应本质是氧化还原反应