 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
已知25℃,φ(Cl2/Cl-)=1.3595V,当氯气的分压是101.325kPa,[C1-]=0.10mol/L时,该电极电位值是()V。
A.1.48
B.42
C.1.30
D.1.24
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.1.48
B.42
C.1.30
D.1.24
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知25℃,φ(Cl2/Cl-)=1.3595V,当氯气的分…”相关的问题
更多“已知25℃,φ(Cl2/Cl-)=1.3595V,当氯气的分…”相关的问题
7.试计算Amm(NH4+)及Amm(Cl-).
已知反应
2Cr3++3Cl2+7H2O=Cr2O72-+6C1-+14H+
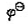 (Cr2O72-/Cr3+)=1.33V,
(Cr2O72-/Cr3+)=1.33V,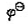 (Cl2/CI-)=1.36V,F=95500J·V-1·mol-2若在298K时组成原电池。
(Cl2/CI-)=1.36V,F=95500J·V-1·mol-2若在298K时组成原电池。
(1)写出该原电监的电池符号,并计算标准电动势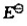 ;(2)计算
;(2)计算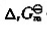 (298K)并判断反应进行的方向;(3)计算标准平衡常数
(298K)并判断反应进行的方向;(3)计算标准平衡常数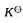 ;(4)若c(H+)=10mol·dm-3,其他离子浓度均为标准浓度,求原电池的电动势E并判断反应进行的方向
;(4)若c(H+)=10mol·dm-3,其他离子浓度均为标准浓度,求原电池的电动势E并判断反应进行的方向
要经过一个由三个Cl-组成的最小三角形窗口(a离子相互不接触).已知NaCl单元晶胞参数a=564pm,r(Cl-)=167pm,r(Na+)=116pm,试计算三角形窗口的半径.
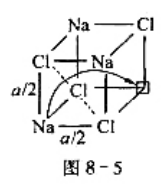
A.0.731
B.0.813
C.0.975
D.0.825
A.0.731
B.0.975
C.0.825
D.0.813
当存在碘催化剂时,氯苯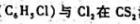 ,溶液中有以下平行二级反应:
,溶液中有以下平行二级反应:
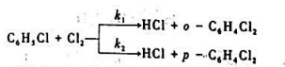
在室温、碘的浓度一定的条件下,当C6H5CI和Cl2在CS2溶液中的初始浓度均为0.5mol.dm-3时,30min后有15%的C6H5CI转化为o-C6H4Cl2有25%的C6H5CI转化为p-C6H4Cl2.试求反应速率常数k1和k2.