 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
根据分子轨道理论,在基态O2分子中能量最高的排布电子的分子轨道是()。
A.#图片0$#
B.#图片1$#
C.#图片2$#
D.#图片3$#
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.#图片0$#
B.#图片1$#
C.#图片2$#
D.#图片3$#
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“根据分子轨道理论,在基态O2分子中能量最高的排布电子的分子轨…”相关的问题
更多“根据分子轨道理论,在基态O2分子中能量最高的排布电子的分子轨…”相关的问题
A.电子在整个分子范围内运动,不再属于某一特定原子
B.反键分子轨道的能量比所有成键分子轨道高,此当反键分子轨道上有电子时,分子不稳定
C.分子轨道是不同原子的原子轨道线性组合面成,杂化轨道是同一原子的原子轨道组合而成
D.只有符合对称性匹配、能量相近和最大重叠原则的原子轨道才能有效地组合成分子轨道
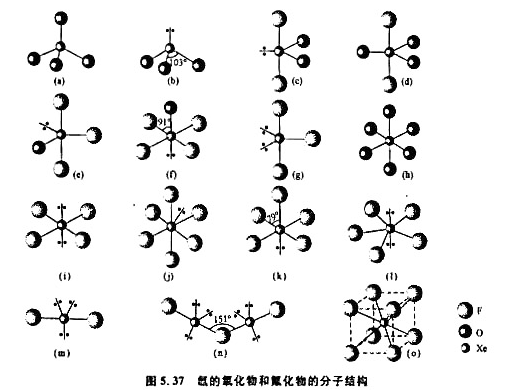
图5.37示出氙的氟化物和氧化物的分子(或离子)结构。
(1)根据图形及VSEPR理论,指出分子的几何构型名称和所属点群;
(2)Xe原子所用的杂化轨道;
(3)Xe原子的表观氧化态;
(4)已知在XeF2,XeF4,加合物晶体中,两种分子的构型与单独存在时的几何构型相同,不会相互化合成XeF2,从中说明什么问题?
某理想气体B的分子基态能级为非简并的,并定为能量的零点,第一激发态能级的能量为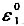 ,其简并度为2.若忽略更高能级,则B的配分函数q=()(写出具体式子).若
,其简并度为2.若忽略更高能级,则B的配分函数q=()(写出具体式子).若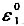 =0.2kT,则第一激发态能级分布数n,与基态能级的分布数n0之比
=0.2kT,则第一激发态能级分布数n,与基态能级的分布数n0之比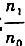 =().
=().
根据下列分子或离子的几何构型,试用杂化轨道理论加以说明.
(1)HgCl2(直线形);(2)SiF4(正四面体);(3)BCl3(平面三角形);
(4)NF3(三角锥形,102°);(5)NO2-(V形,115.4°);(6)SiF62-(八面体).
A.凡中心原子采取sp3杂化轨道成键的分子其几何构型都是正四面体
B.CH4分子中的sp3杂化轨道是由4个H原子的1s轨道和C原子的2p轨道混合而成的
C.sp3杂化轨道是由同原子中能量相近的s轨道和p轨道混合起来形成的一组能量相等的新轨道
D.凡AB3型的共价化合物,其中心原子A均采用sp3杂化轨道成键
(2007年)用杂化轨道理论推测下列分子空间构型,其中为平面三角形的是()。
A.NF3
B.AsH3
C.BF3
D.SbH3