 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
称取纯的四草酸氢钾(KHC2O4·H2C2O4·2H2O)0.6174g,用NaOH标准溶液滴定时,用去26.35mL.求NaOH溶液的浓度.
称取纯的四草酸氢钾(KHC2O4·H2C2O4·2H2O)0.6174g,用NaOH标准溶液滴定时,用去26.35mL.求NaOH溶液的浓度.
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“称取纯的四草酸氢钾(KHC2O4·H2C2O4·2H2O)0…”相关的问题
更多“称取纯的四草酸氢钾(KHC2O4·H2C2O4·2H2O)0…”相关的问题
称取含NaCl试样0.5000g,溶解后加入纯AgNO3固体0.8920g,用Fe3+作指示剂,剩余的AgNO3用0.1400mol/L的KSCN溶液回滴,用去23.50ml。求试样中NaCl的质量分数。(试样中除Cl-外,不含有与Ag+生成沉淀的其他物质的离子,MAgNO3=169.9)
2
O3等杂质).将不纯的SiO2用H2SO4-HF.处理,使SiO2转化为SiF4而除去.残渣经灼烧后,其质量为0.0013g.计算试样中纯SiO2的含量.若不经H2SO4-HF处理,杂质造成的误差有多大?
(1)实际上所配缓冲溶液的pH为多少?
(2)若要配制pH=0.64三氯乙酸缓冲溶液。需加入多少摩尔强酸或强碱?
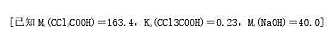
完成并配平下列化学反应方程式。
(1)金属铬缓慢地溶于盐酸。
(2)三氧化二铬与氯酸钾共熔。
(3)三氧化二铬与硫酸氢钾共熔。
(4)三氧化铬受热分解。
(5)向+3价铬盐的溶液中加入硫化钠溶液。
(6)高温下三氧化二铬与硅反应。
(7)加热铬酸钠与焦炭的混合物。
(8)将重铬酸钾加到氢溴酸中。
(9)重铬酸钾与氯化钾混合后,滴加浓硫酸并加热。
(10)三氧化钼溶于热的浓氨水。
(11)单质锰与热水反应。
(12)硫化锰沉淀在空气中放置。
(13)固体硝酸锰受热分解。
(14)硫酸锰溶液与高锰酸钾溶液混合并充分反应。
(15)二氧化锰、氢氧化钾与氯酸钾混合后高温共熔。
(16)锰酸钾溶液中加稀硫酸。
(17)高锰酸钾晶体在200℃下分解。
(18)高锰酸盐在碱性溶液中与亚硫酸盐作用。
(19)用高锰酸钾溶液标定草酸溶液。