 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
关于反应C(s)+H2O(g)⇌CO(g)+H2(g)的平衡常数的书写形式,正确的是()
A.K
B.K
C.K
D.K
 答案
答案
C、K
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.K
B.K
C.K
D.K
 答案
答案
C、K
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“关于反应C(s)+H2O(g)⇌CO(g)+H2(g)的平衡…”相关的问题
更多“关于反应C(s)+H2O(g)⇌CO(g)+H2(g)的平衡…”相关的问题
已知反应SnO2(s)+2H2(g)=Sn(s)+2H2O(g)和CO(g)+H2O(g)=CO2(g)+H2(g)的平衡常数分别为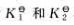 。则反应SnO2(s)+2CO(g)=2CO2(g)+Sn(s)
。则反应SnO2(s)+2CO(g)=2CO2(g)+Sn(s)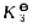 的=()。
的=()。
试用热力学数据表计算823K下以下反应的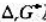 及
及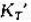 :
:
(1)CoO(s)+H2(g)=Co(s)+H2O(g)
(2)CoO(s)+CO(g)=Co(s)+CO2(g)
并讨论H2和CO还原CoO为Co的可能性,你以为哪种方法更好一些?为什么?
A.生成1molCO的同时生成1molH2
B.容器中物质的总质量不发生变化
C.n(H2O):n(H2)=1 :1
D.v逆(H2O)=v正(CO)
A.当v(CO)(正)=v(H2)(正),时,反应达到平衡状态
B.其他条件不变,适当增加C(s)的质量会使平衡正向移动
C.保持容器体积不变,充入少量He使体系压强增大,反应速率一定增大
D.其他条件不变,仅将容器的体积缩小一半,再次达到平衡时,H20(g)的平衡浓度可能是原来的2.1倍
A.CO2(g)+CaO(s)→CaCO3(s)
B.H2(g)+I2(g)→HI(g)
C.H2(g)+Cl2(g)→2HCl(g)
D.H2(g)+O2(g)→H2O(g)
A.3,2
B.3,1
C.1,0
D.2,1
A.v(NH3)=0.01 mol·L−1·s−1
B.v(O2)=0.001 mol·L−1·s−1
C.v(NO)=0.001 mol·L−1·s−1
D.v(H2O)=0.045 mol·L−1·s−1