 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
某一弱酸HA的Ka=2x10-5,它在某种有机溶剂和水中的分配系教为30.0,当水溶液的(1)pH=1;(2)p=5时,分配比各为多少?用等体积的有机溶剂萃取,萃取效率各为多少?
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某一弱酸HA的Ka=2x10-5,它在某种有机溶剂和水中的分…”相关的问题
更多“某一弱酸HA的Ka=2x10-5,它在某种有机溶剂和水中的分…”相关的问题
准确量取30.00ml弱酸,加水稀释至100ml。以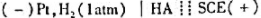 为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
(1)弱酸HA的Ka。
(2)原弱酸HA的浓度。
已知电池PtH2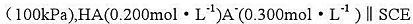 测得E=0.672V.计算弱酸HA的离解常数(忽略液接电位).
测得E=0.672V.计算弱酸HA的离解常数(忽略液接电位).
A.羟氨(NH2OH)(Kb=1.0×10-9)
B.氨水(NH3的Kb=1.8×10-5)
C.醋酸(Ka=1.8×10-5)
D.甲酸(Ka=1×10-4)CH2OOH
A.6.0~10.7
B.6.0~9.7
C.7.0~10.7
D.8.0~9.7
由一元弱酸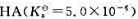 和它的共轭碱NaA组成的缓冲溶液中,HA的浓度为0.25mol·L-1.若在100mL此缓冲溶液中加入5.0mmolNaOH固体,溶液的pH变为5.60。计算加入NaOH固体前缓冲溶液的pH.
和它的共轭碱NaA组成的缓冲溶液中,HA的浓度为0.25mol·L-1.若在100mL此缓冲溶液中加入5.0mmolNaOH固体,溶液的pH变为5.60。计算加入NaOH固体前缓冲溶液的pH.
A.溶液的pH越高,弱酸共轭碱型体的分布系数越大
B.当两型体的分布系数相等时,溶液的pH=pKa
C.分布系数是Ka的函数
D.分布系数取决于物质的性质、溶液的酸度和总浓度