 更多“经转氨基作用生成的氨(NH3)对机体来说是一种有毒物质,体内…”相关的问题
更多“经转氨基作用生成的氨(NH3)对机体来说是一种有毒物质,体内…”相关的问题
A.促进胃肠运动,排毒增力
B.乳果糖呈酸性,增加氨排出
C.使肠内呈酸性,减少氨的形成和吸收
D.乳果糖与NH3结合
E.分解为乳糖、果糖、氨生成减少
A.该反应属于复分解反应
B.该反应利用了NH3的强氧化性
C.若管道漏气遇氨就会产生白烟
D.生成1 mol N2有3 mol电子转移
A.蓝色沉淀溶解的离子方程式为Cu(OH)2+4NH3·H2O=[Cu(NH3)4]2++2OH-+4H2O
B.NH3极易溶于水是因为氨分子间易形成氢键
C.硫酸四氨合铜在乙醇中的溶解度小于在水中的溶解度
D.NH3比H2O更容易与Cu2+反应形成配合物
A.氨气、液氨、氨水的成分相同,均为纯净物
B.蘸有浓盐酸的玻璃棒与蘸有浓氨水的玻璃棒相互靠近,有白烟生成
C.氨气的密度比空气小,可以采用向上排空气法或排水集气法收集
D.氨水中含氮元素的微粒有NH3和NH3·H2O两种
A.v(H2)=0.1mol·(L·min)-1
B.v(N2)=0.1mol·(L·min)-1
C.v(N2)=0.2mol·(L·min)-1
D.v(NH3)=0.3mol·(L·min)-1
的HCL中,过量的用0.5000mol/L的NaOH回滴,用去1.56ml,试样中NH3的质量
分数W(NH3)为()(M(NH3)=17.03)。
A.41.25﹪
B.41.2﹪
C.40.01﹪
D.41.0﹪
A.精氨酸参与尿素循环的机制,增加肝精氨酸酶活性,促进尿素生成,持久降氨
B.精氨酸参与三羧酸循环的机制,增加肝精氨酸酶活性,促进尿素生成,持久降氨
C.谷氨酸与NH3快速结合形成谷氨酰胺,增强外周组织对氨转运,快速降氨
D.谷氨酸与NH3快速结合形成谷氨酰胺,增强血液对氨转运,快速降氨
某校化学研究性学习小组的同学在学习了氨的性质后讨论:运用类比的思想,既然氨气具有还原性,能否像H2那样还原Cu0呢?他们设计实验制取氮气并探究上述问题。请你参与该小组的活动并完成下列研究:
(一)制取氨气
(1)写出实验制取氨气的化学方程式()。
(2有同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气。你认为他能否达到目的()(填“能”或“否”)。理由是()。
(二)该小组中某同学设计了下图所示的实验装置(夹持及尾气处理装置未画出),探究氨气的还原性: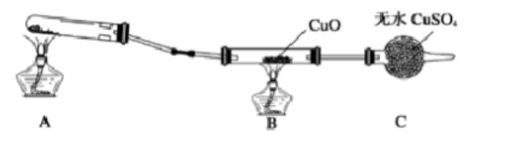 ⑴该装置在设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是:()。
⑴该装置在设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是:()。
(2)利用改进后的装置进行实验,观察到Cu0变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体。写出氨气与Cu0反应的化学方程式()。
(三)问题讨论:
有同学认为:NH3与Cu0反应生成的红色物质中可能含有Cu20.已知:Cu20是一种碱性氧化物;在酸性溶液中,Cu'的稳定性差(Cu+→Cu+Cu2+)。请你设计一个简单的实验检验该红色物质中是否含有Cu0:()。


 如果结果不匹配,请
如果结果不匹配,请 

















