 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
价层电子构型满足下列条件之一的是哪一类或哪一个元素? (1)具有2个p电子; (2)有2个量子数为n=4
价层电子构型满足下列条件之一的是哪一类或哪一个元素? (1)具有2个p电子; (2)有2个量子数为n=4和l=0的电子,6个量子数为n=3和l=2的电子; (3)3d为全充满,4s只有1个电子的元素。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
价层电子构型满足下列条件之一的是哪一类或哪一个元素? (1)具有2个p电子; (2)有2个量子数为n=4和l=0的电子,6个量子数为n=3和l=2的电子; (3)3d为全充满,4s只有1个电子的元素。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“价层电子构型满足下列条件之一的是哪一类或哪一个元素? (1)…”相关的问题
更多“价层电子构型满足下列条件之一的是哪一类或哪一个元素? (1)…”相关的问题
试用价层电子对互斥理论判断下列分子或离子的空间构型:

要求写出中心原子提供的价层电子数、配体提供的电子数、离子提供的电子数、价层电子总数、价层电子对数、电子对构型和分子(离子)构型。
X、Y、Z、R为前四周期原子序数依次增大的元素。X原子有3个能级,且每个能级上的电子数相等;Z原子的不成对电子数在同周期中最多,且Z的气态氢化物在同主族元素的氢化物中沸点最低;X、Y、R三元素在周期表中同族。
(1)R元素基态原子的价层电子排布式为()。
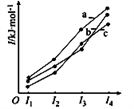
(2)下图表示X、Y、Z的四级电离能变化趋势,其中表示Y的曲线是()(填标号)。
 (3)化合物(XH2=X=O)分子中X原子杂化轨道类型分别是(),1mol(X2H5O)3Z=O分子中含有的σ键与π键的数目比为()。
(3)化合物(XH2=X=O)分子中X原子杂化轨道类型分别是(),1mol(X2H5O)3Z=O分子中含有的σ键与π键的数目比为()。
(4)Z与氯气反应可生成一种各原子均满足8电子稳定结构的化合物,其分子的空间构型为()。
(5)某R的氧化物立方晶胞结构如图所示,该物质的化学式为()。(用元素符号表示),已知该晶体密度为ρg/cm3,距离最近的原子间距离为dpm,则R的相对原子质量为()。(阿伏加德罗常数为NA)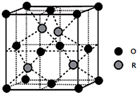
A.价层电子对互斥模型可用来预测分子的空间构型
B.分子中价电子对相互排斥决定了分子的空间构型
C.中心原子上的孤电子对也要占据中心原子周围的空间并参与互相排斥
D.分子中键角越大,价电子对相互排斥力越大,分子越稳定
A.若n=2,则分子的立体构型为V形
B.若n=3,则分子的立体构型为三角锥形
C.若n=4,则分子的立体构型为正四面体形
D.以上说法都不正确
A.施工单项合同估算价在200万元人民币以上的
B.设备、材料等货物的采购,单项合同估算价在100万元以上的
C.勘察、设计、监理等服务的采购,单项合同估算价在50万元人民币以上的
D.办公用品年采购额在5万元以上的