 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某反应25°C时K=32,37℃时K=50.求37℃时该反应的(设此温度范围内为常数)
某反应25°C时K=32,37℃时K=50.求37℃时该反应的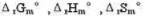 (设此温度范围内为常数)
(设此温度范围内为常数)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某反应25°C时K=32,37℃时K=50.求37℃时该反应的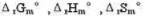 (设此温度范围内为常数)
(设此温度范围内为常数)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某反应25°C时K=32,37℃时K=50.求37℃时该反应…”相关的问题
更多“某反应25°C时K=32,37℃时K=50.求37℃时该反应…”相关的问题
某一气相反应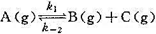 ,已知在298 K时,k1=0.21s-1,k-2=5×10-9Pa-1·s-1,当温度由298 K升到310 K时,k和k-2的值均增加1倍,试求:
,已知在298 K时,k1=0.21s-1,k-2=5×10-9Pa-1·s-1,当温度由298 K升到310 K时,k和k-2的值均增加1倍,试求:
(1)298K时的反应平衡常数Kp;
(2)正、逆反应的实验活化能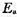 ;
;
(3)298K时反应的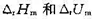 ;
;
(4)在298K时,A的起始压力为100kPa,若使总压力达到152kPa,所需的时间。
A.正反应的活化能与逆反应的活化能相等
B.正反应的活化能大于逆反应的活化能
C.逆反应的活化能大于正反应的活化能
D.无法比较正、逆反应的活化能的相对大小
某一气相反应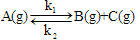 ,已知在298 K时,k1=0.21s-1,k-2=5×10-9Pa-1·s-1,当温度由298K升到310K时,k1和k-2的值均增加1倍,试求:
,已知在298 K时,k1=0.21s-1,k-2=5×10-9Pa-1·s-1,当温度由298K升到310K时,k1和k-2的值均增加1倍,试求:
(1)298K时的反应平衡常数Kp
(2)正,逆反应的实验活化能Ea
下列电池的电动势为0.981V。Zn|Zn2+(5.0×10-3mol/L),NH3(0.12mol/L) SHE计算下述反应的平衡常数K(25℃时)。
SHE计算下述反应的平衡常数K(25℃时)。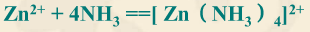
28. 反应A+2B→D的速率方程为-dcA/dt=kcAcB,25℃时K=2×10-4dm3·mol-1·s-1。(1)若初始浓度cA,0=0.02mol·dm-3,cB,0=0.04mol·dm-3,求t1/2?(2)若将反应物A与B的挥发性固体装入5dm3的密闭容器中,已知25℃时A,B的饱和蒸气压分别为10kPa和2kPa,问25℃时0.5mol的A转化为产物需要多长时间?
A.K越大,达到平衡时反应进行的程度越大
B.K越大,达到平衡时反应物的转化率越大
C.K随反应物浓度的改变而改变
D.K随温度的改变而改变