题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
聚合硫酸铁【Fe(OH)SO4】n能用作净水剂(絮凝剂),可由绿矾(FeSO4·7H2O)和KClO3在水溶液中反应得到。下列说法不正确的是()
A.KClO3作氧化剂,每生成1 mol [Fe(OH)SO4]n消耗6/n mol KClO3
B.生成聚合硫酸铁后,水溶液的pH增大
C.聚合硫酸铁可在水中形成氢氧化铁胶体而净水
D.在相同条件下,Fe3+比[Fe(OH)]2+的水解能力更强
 答案
答案
A、KClO3作氧化剂,每生成1 mol [Fe(OH)SO4]n消耗6/n mol KClO3
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案

 更多“聚合硫酸铁【Fe(OH)SO4】n能用作净水剂(絮凝剂),可…”相关的问题
更多“聚合硫酸铁【Fe(OH)SO4】n能用作净水剂(絮凝剂),可…”相关的问题
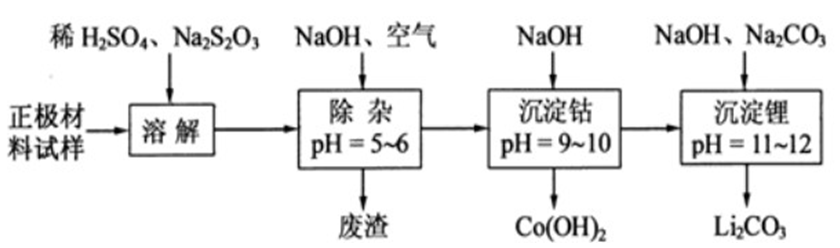
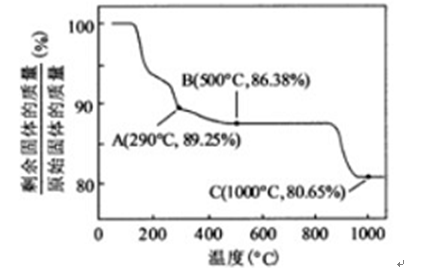
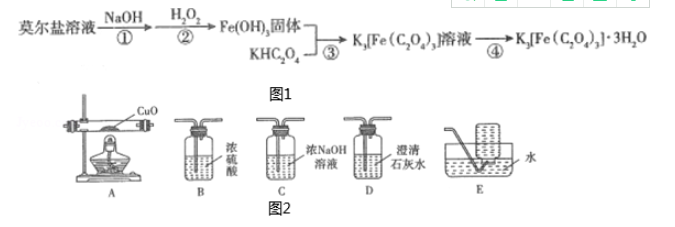 。回答下列问题:
。回答下列问题: