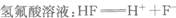题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列离子方程式书写不正确的是()
A.盐酸与Na2CO3溶液混合:CO32- + 2H+ = CO2↑+H2O
B.l2和H2O反应:Cl2+H2O = 2H+ + Cl- + ClO-
C.NO2通入水中:H2O+3NO2=2H+ + 2NO3- + NO
D.浓盐酸和二氧化锰共热制Cl2:MnO2 + 4H+ + 2Cl- = Mn2+ + Cl2↑+ 2H2O
 答案
答案
B、l2和H2O反应:Cl2+H2O = 2H+ + Cl- + ClO-
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案

 更多“下列离子方程式书写不正确的是()”相关的问题
更多“下列离子方程式书写不正确的是()”相关的问题