 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某原电池的电池反应为Fe+2Fe3+=3Fe2+,与此电池反应不符合的原电池是()①铜片、铁片、FeCl3溶液组成的原电池 ②石墨、铁片、Fe(NO3溶液组成的原电池 ③铁片、锌片、Fe2(SO3溶液组成的原电池 ④银片、铁片、Fe(NO2溶液组成的原电池
A.①②
B.②③
C.③④
D.②④
 答案
答案
C、③④
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.①②
B.②③
C.③④
D.②④
 答案
答案
C、③④
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某原电池的电池反应为Fe+2Fe3+=3Fe2+,与此电池反…”相关的问题
更多“某原电池的电池反应为Fe+2Fe3+=3Fe2+,与此电池反…”相关的问题
A.Sn2++2H+Sn4++H2
B.Sn4++H2Sn2++2H+
C.Sn4++2H+Sn2++H2
D.Sn2++H2Sn4++2H+
A.锌为正极,Ag2O为负极
B.原电池工作时,负极区PH增大
C.原电池工作时,负极区PH增大,正极区PH减小
D.锌为负极:Zn+2OH--2e- =ZnO+H2O
A.无论a和b是否连接均可形成原电池
B.和b不连接时,铁片上会有金属铜析出
C.和b用导线连接时,铜片上发生的反应为Cu2++2e-= Cu
D.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色
A.正极的电极反应为O2+2H2O+2e﹣=4OH﹣
B.负极的电极反应为Al+3OH﹣﹣﹣3e﹣═AI(OH)3↓
C.电池工作过程中,电解液的pH保持不变
D.电池使用时可能析出H2并放热
A.放电时负极反应为Zn-2e-+2OH-=Zn(OH)2
B.充电时阳极反应为Fe(OH)3-3e-+5OH-=FeOeq \o\al(2-,4)+4H2O
C.放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化
D.放电时正极附近溶液的碱性增强
某化学兴趣小组设计了如图所示的电化学装置,下列说法不正确的是()。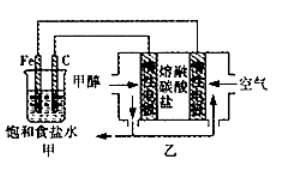
A.乙池工作时,CO32―不断移向负极
B.乙池负极反应为CH3OH-6e一+3CO32―=4CO2+2H2O
C.甲池中Fe电极发生的反应为2Cl―-2e一=Cl2
D.为了使电池持续供电,工作时必须有CO2参与循环
A.电池工作时,COeq \o\al(2-,3)向负极移动
B.电池放电时,电子经外电路由通氧气的正极流向通氢气的负极
C.正极的电极反应为4OH--2e-===O2↑+2H2O
D.通氧气的电极为正极,发生氧化反应
A.铂做成网状的目的是为了节省铂的用量
B.正极反应式为:O2+2H2O+4e﹣=4OH﹣
C.电池工作时,阴离子向负极移动
D.该电池的一大优点是只需更换铝板就可继续使用
A.正极反应式为O2+2H2O+4e-=4OH-
B.电池工作时,电流由铝电极沿导线流向铂电极
C.以网状的铂为正极,可增大与氧气的接触面积
D.该电池通常只需更换铝板就可继续使用
A.X>Z>Y>W
B.Z>W>X>Y
C.Z>Y>X>W
D.Z>X>Y>W