 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
NH5属于离子晶体。与水反应的化学方程式为:NH5+H2O→NH3·H2O+H2↑,它也能跟乙醇发生类似的反应,并都产生氢气。有关NH5叙述正确的是()
A.与乙醇反应时,NH5被氧化
B.NH5中N元素的化合价为+5价
C.1 mol NH5中含有5 molN—H键
D.1 mol NH5与H2O完全反应,转移电子2 mol
 答案
答案
A、与乙醇反应时,NH5被氧化
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.与乙醇反应时,NH5被氧化
B.NH5中N元素的化合价为+5价
C.1 mol NH5中含有5 molN—H键
D.1 mol NH5与H2O完全反应,转移电子2 mol
 答案
答案
A、与乙醇反应时,NH5被氧化
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“NH5属于离子晶体。与水反应的化学方程式为:NH5+H2O→…”相关的问题
更多“NH5属于离子晶体。与水反应的化学方程式为:NH5+H2O→…”相关的问题
A.1 molNH5 中含有 4NA个N—H 键(NA表示阿伏加德罗常数)
B.NH5中既有共价键又有离子键
C.NH5中的氢离子的电子层排布与Li+不相同
D.它与水反应的化学方程式为:NH5+H2O=NH3·H2O+H2↑
K3[Fe(C2O4)3]•3H2O(三草酸合铁酸钾)为亮绿色晶体,易溶于水,难溶于乙醇,是制备负载型活性铁催化剂的主要原料。实验室用莫尔盐[(NH4)2Fe(SO4)2•6H2O]制备K3[Fe(C2O4)3]•3H2O的流程如图1所示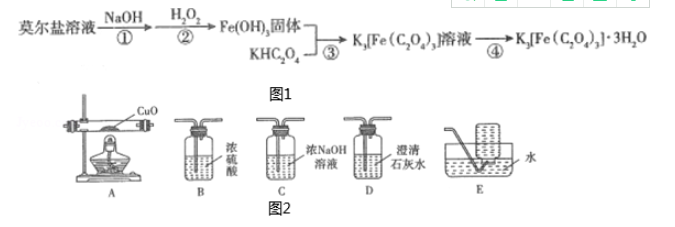 。回答下列问题:
。回答下列问题:
问题1、K3[Fe(C2O4)3]中铁离子的配位数为,其配体C2O42﹣中C原子的杂化方式为()。
问题2、步骤②发生反应的化学方程式为()。
问题3、步骤③将Fe(OH)3加入到KHC2O4溶液中,水浴加热,控制溶液pH为3.0~3.5,随反应进行需加入适量()。(已知:常温下KHC2O4溶液的pH约为3.5)
问题4、得到的三草酸合铁酸钾晶体依次用少量冰水、95%乙醇洗涤的目的是()。
问题5、某研究小组将K3[Fe(C2O4)3]•3H2O在一定条件下加热分解,利用图2装置(可重复使用)验证所得气体产物中含有CO和CO2。 ①按气流从左到右的方向,依次连接的合理顺序为()。(填装置序号) ②确认气体产物中含CO的现象()。
粉煤灰是一种火山灰质材料,来源于煤中的无机组成,从粉煤灰中能够获得Al2O3,已知某火力发电厂的粉煤灰中的化学成分如下表。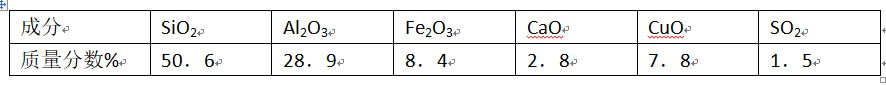 问题一、上述氧化物中能与水反应的是()。
问题一、上述氧化物中能与水反应的是()。
问题二、从粉煤灰中提取Al¬2O3的一种工艺流程如下:
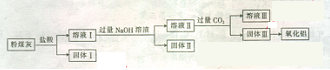
①体I中含有的主要物质的化学式为()。
②溶液Ⅱ中通人过量的CO2,发生反应的离子方程式为()。
问题三、氧化铝和焦炭的混合物与氮气在高温下反应,可制得新型非金属材料A1N与一种中学常见气体x。已知每转移3mol-,就有1.5mol化合物X生成,此反应的化学方程式为()。
超细纳米铜粉的比表面积大、表面活性中心数目多,在冶金和石油化工中是优良的催化剂。利用铜屑制备超细纳米铜粉的工艺流程如下: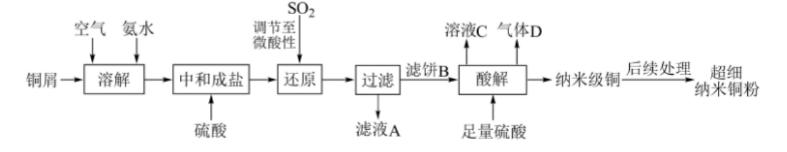 回答下列问题:
回答下列问题:
(1)“溶解”的离子方程式为(),为了加快“溶解”反应,可采取的措施有()(写出一种即可)。
(2)“滤饼B”是一种白色晶体,元素分析表明含有Cu、S、O、N、H五种元素,Cu、S、N的原子数目比为1:1:1,光谱分析显示所含阴离子呈三角锥形,其中一种阳离子呈正四面体形,则该晶体的化学式为()。
(3)“酸解”的化学方程式为();验证酸解后所得铜粉为纳米级的简便方法是()(填操作及现象)。
(4)“溶液C”可以循环利用,应将其导入到()操作中(填操作单元的名称)。
如图所示中,A是一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应的火焰均呈黄色。
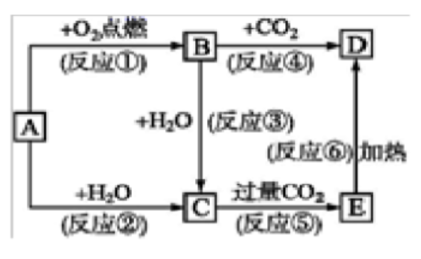 填写下列空白:
填写下列空白:
(1)写出化学式:A(),B(),D()。
(2)以上反应中属于氧化还原反应的有()(填序号)。
(3)写出反应⑤的离子方程式:()。
写出反应⑥的化学方程式:()。
无水AlCl3可用作有机合成的催化剂、食品膨松剂等。工业上由铝土矿(主要成分是A12O3和Fe2O3)和石油焦(主要成分是C)按以下图所示流程进行一系列反应来制备无水AlCl3。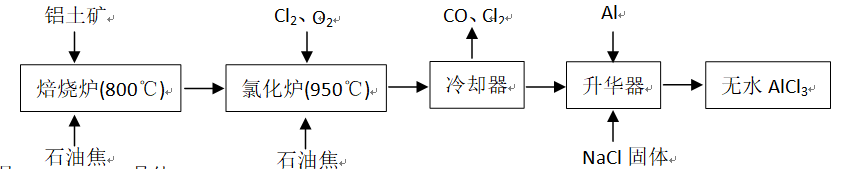
问题一、AlCl3是()晶体。
问题二、氯化炉中Al2O3、C12和C反应的化学方程式是()。
问题三、冷却器排出的尾气中含有大量CO和少量Cl2,需用Na2SO3溶液除去Cl2,写出此反应的离子方程式是()。
问题四、升华器中主要含有AlCl3和FeCl3,需加入少量Al,其作用是()。
问题五、为测定无水AlCl3产品的纯度,现称取16.25g精制后的无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,其残留固体质量为0.32g。则AlCl3产品的纯度为()。
以粉煤灰(主要含Al2O3、SiO2,还有少量的Fe2O3)为原料制取Al2O3的流程如下: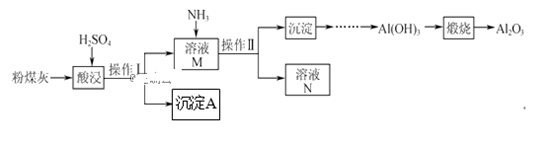 (1)操作Ⅰ的名称是()。
(1)操作Ⅰ的名称是()。
(2)用H2SO4“酸浸”时的离子方程式为()(任写一个)。
(3)简述如何检验酸浸后溶液中是否有Fe3+()。
(4)“煅烧”时的化学方程式为()。
(5)沉淀A与氢氟酸反应的化学方程式为()。
工业上用铝土矿(主要成分为氧化铝,含少量氧化铁)制取铝的过程如图所示: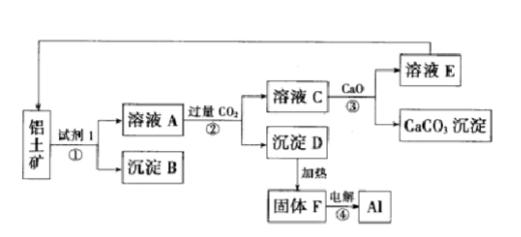 请回答:
请回答:
(1)试剂Ι为()(填化学式),①-④转化中属于氧化还原反应的是()(填序号);
(2)沉淀B的化学式为(),写出该物质发生铝热反应的化学方程式();
(3)电解F,当转移0.6mol,电子时,可制得铝()g;
(4)沉淀D是药物“胃舒平”的主要成分,可用于治疗胃酸(稀盐酸)过多,写出该反应的离子方程式();
(5)②中发生反应的离子方程式为()。
(1表示氯碱工业生产原理的化学方程式为()。
(2)X的另一种氢化物X2H4可作为火箭推进器燃料,其结构式为()。
(3)Y的氧化物中,有一种既含离子键又含共价键,该氧化物的电子式为()。
(4)Z的氧化物属于晶体,工业制备Z单质的化学方程式为()。
(5)W单质是毒性很大的窒息性气体。工业上用X气态氢化物的浓溶液检验W单质是否泄露,写出反应的化学方程式()。