 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
取0.1000mol/LNaCl溶液30.00ml,加入0.1000mol/LAgNO3溶液50.00ml,以铁铵矾作指示剂,用0.10
00mo/LNH4SCN溶液滴定过量的Ag+,在终点时Fe3+的浓度为0.015mol/L。因为没有采取防止AgCl转化成AgSCN的措施,滴定至稳定的红色不再消失作为终点,此时FeSCN2+的浓度6.4x10-6mol/L,计算滴定误差(已知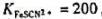
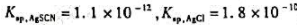 )
)
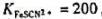
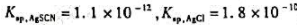 )
)
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“取0.1000mol/LNaCl溶液30.00ml,加入0.…”相关的问题
更多“取0.1000mol/LNaCl溶液30.00ml,加入0.…”相关的问题
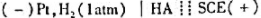 为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算: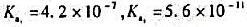 )
)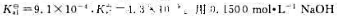 溶液滴定0.1000mol·L-1酒石酸溶液时.在滴定曲线上可出现()个突跃范围.可选择()作指示剂。
溶液滴定0.1000mol·L-1酒石酸溶液时.在滴定曲线上可出现()个突跃范围.可选择()作指示剂。
















