 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
298K时,将某可逆电池短路使其放电Imol电子的电量,此时放电的热量恰好等于该电池可逆操作时所
吸收热量的40倍.试计算此电池的电动势。已知此电池电动势的温度系数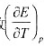
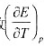
为1.40x10-4V/K。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
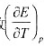
为1.40x10-4V/K。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“298K时,将某可逆电池短路使其放电Imol电子的电量,此时…”相关的问题
更多“298K时,将某可逆电池短路使其放电Imol电子的电量,此时…”相关的问题
B、课本要求
C、如果先连接负极电缆,那么在连接正极电缆时,万一扳手搭铁造成畜电池短路放电,不仅放电电流大会大量火花,而且还有引着蓄电池产生的氢气而发生爆炸的危险
D、如果先连接负极电缆,那么在连接正极电缆时,万一扳手搭铁造成蓄电池断路放电,不仅放电电流大会产生大星火花而且还有引着蓄电池产生的氢气而发生爆炸的危险
A.极板材料或电解质中有杂质,形成闭合“局部电池”耗能电能
B.隔板破裂或活性物质脱落
C.蓄电池盖上有电解液或水,正、负极桩短路
D.蓄电池长期存放电解液中硫酸下沉,引起放电
E.蓄电池容量过高
298K时,已知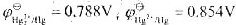 ,试计算(1)反应Hg2++e→1/2Hg22+的标准电极电势。(2)为反应Hg+Hg2+→Hg2-设计电池,并计算该反应的标准平衡常数。
,试计算(1)反应Hg2++e→1/2Hg22+的标准电极电势。(2)为反应Hg+Hg2+→Hg2-设计电池,并计算该反应的标准平衡常数。
已知反应
2Cr3++3Cl2+7H2O=Cr2O72-+6C1-+14H+
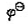 (Cr2O72-/Cr3+)=1.33V,
(Cr2O72-/Cr3+)=1.33V,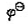 (Cl2/CI-)=1.36V,F=95500J·V-1·mol-2若在298K时组成原电池。
(Cl2/CI-)=1.36V,F=95500J·V-1·mol-2若在298K时组成原电池。
(1)写出该原电监的电池符号,并计算标准电动势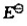 ;(2)计算
;(2)计算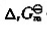 (298K)并判断反应进行的方向;(3)计算标准平衡常数
(298K)并判断反应进行的方向;(3)计算标准平衡常数 ;(4)若c(H+)=10mol·dm-3,其他离子浓度均为标准浓度,求原电池的电动势E并判断反应进行的方向
;(4)若c(H+)=10mol·dm-3,其他离子浓度均为标准浓度,求原电池的电动势E并判断反应进行的方向