 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
实验室使用的石蕊化学式为,在物质分类上属于()。
A.氧化物
B.有机小分子化合物
C.有机高分子化合物
D.含氧化合物
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.氧化物
B.有机小分子化合物
C.有机高分子化合物
D.含氧化合物
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“实验室使用的石蕊化学式为,在物质分类上属于()。”相关的问题
更多“实验室使用的石蕊化学式为,在物质分类上属于()。”相关的问题
工业上用铝土矿(成分为氧化铝、氧化铁)制取铝的过程如下:
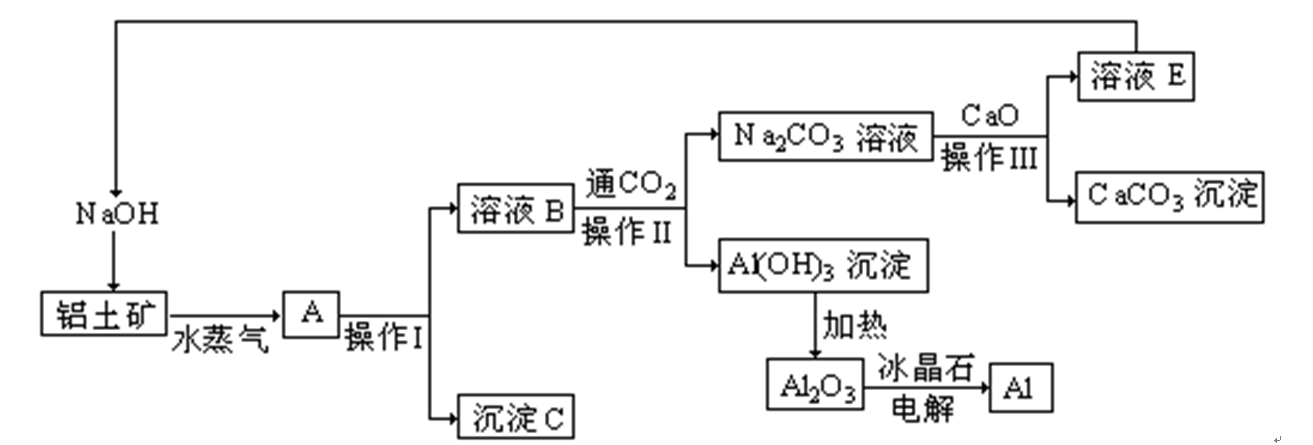 请答复以下问题:
请答复以下问题:
问题一、水蒸气的作用()。
问题二、沉淀C的化学式为(),该物质除了用于金属冶炼以外,还可用作()。
问题三、操作I、操作II、操作III都用到的玻璃仪器是有()。
问题四、实验室洗涤Al(OH)3沉淀应该如何操作:()。
问题五、生产过程中,除NaOH、H2O可以循环使用外,还可以循环使用的物质有()(填化学式)。用此法制取铝的副产品是()(填化学式)。
十二水合硫酸铝钾[KAI(SO4)2・12H2O]俗名明矾,在生活、医药、工业上应用广泛。下面是实脸室探究从铝土矿(主要成分是氧化铝,含少量氧化铁和二氧化硅杂质)制备明矾的流程示意图。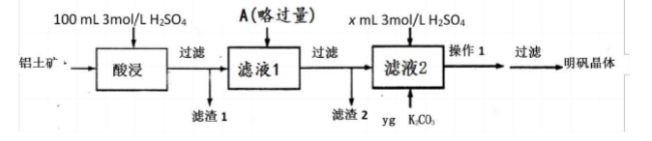 已知:二氧化硅不溶于水,也不与硫酸反应。
已知:二氧化硅不溶于水,也不与硫酸反应。
(1)铝元素在地壳中以()态存在,写出KAl(SO4)·12H2O溶于水的电离方程式()。当明矾溶液中混有NaCl时,简述如何检验Cl()。
(2)滤渣1主要为()(填化学式);以Al2O3为原料,制备该单质铝的反应方程式()。
(3)若A为金属单质,则滤渣2的成分有()。
(4)操作1是蒸发溶剂至有大量晶膜、冷却结晶。实验室进行该操作时,需要的实验仪器有铁架台、()。
(5)如图为某硫酸试剂瓶的标签。若用其配制100mL3mol/L的溶液,需该硫酸()mL(含ρ的表达式)。若此硫酸物质的量浓度为c1,35%的硫酸物质的浓度为c2,则c1()2c2(填大于,小于或等于)。 (6)工业生产中,获取明矾晶体后的母液应该()(填序号)。
(6)工业生产中,获取明矾晶体后的母液应该()(填序号)。
A、弃去
B、返回酸浸流程重复利用
C、返回滤液1重复利用
D、返回滤液2重复利用
KMnO4是一种重要消毒剂,俗名叫灰锰氧。
Ⅰ.某工厂以废旧锌锰电池为原料制备高锰酸钾的流程如下(部分产物已省略)
回答下列问题: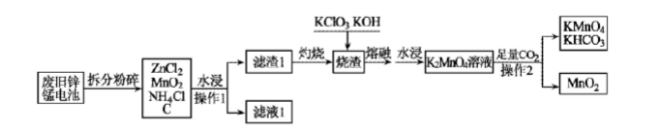 (1)K+的结构示意图为()。
(1)K+的结构示意图为()。
(2)这种锌锰电池放电时,负极的电极反应式为()。
(3)滤渣1“灼烧”的目的是();可循环利用的物质是()(填化学式)。
(4)“水浸”采用适当加热搅拌等措施,其目的是(),熔融“烧渣”可能产生的大气污染物是()。
(5)向K2MnO4溶液中通入足量CO2的离子方程式为:()。
Ⅱ.实验室中利用K2MnO4进行如下实验,下列说法错误的是()。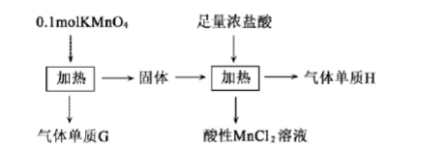 A、G与H均为氧化产物
A、G与H均为氧化产物
B、实验中KMnO4只作氧化剂
C、Mn元素至少参与了3个氧化还原反应
D、G与H的物质的量之和可能为0.25mol
高纯二氧化硅可用来制造光纤。某蛇纹石的成分见下表: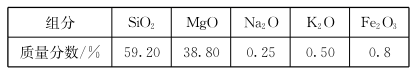 通过下图流程可由蛇纹石制备较纯净的二氧化硅。
通过下图流程可由蛇纹石制备较纯净的二氧化硅。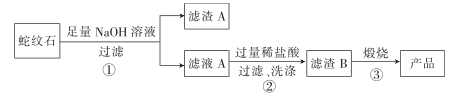 (1)蛇纹石中涉及的可溶性金属氧化物有()(写化学式)。
(1)蛇纹石中涉及的可溶性金属氧化物有()(写化学式)。
(2)步骤①中涉及SiO2 反应的离子方程式为()。
(3)滤渣 A的成分有()(填化学式)。
(4)步骤②中洗涤沉淀的方法是()。
(5)步骤③反应的化学方程式为();实验室进行步骤③需要用到的仪器有坩埚、泥三角、酒精灯、玻璃棒、()和()。
工业上用铝土矿(主要成分为氧化铝,含少量氧化铁)制取铝的过程如图所示: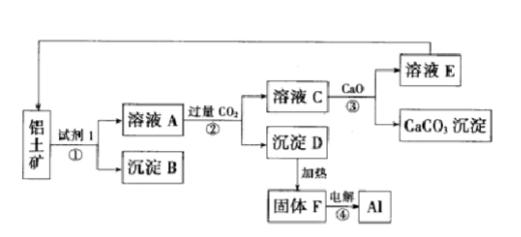 请回答:
请回答:
(1)试剂Ι为()(填化学式),①-④转化中属于氧化还原反应的是()(填序号);
(2)沉淀B的化学式为(),写出该物质发生铝热反应的化学方程式();
(3)电解F,当转移0.6mol,电子时,可制得铝()g;
(4)沉淀D是药物“胃舒平”的主要成分,可用于治疗胃酸(稀盐酸)过多,写出该反应的离子方程式();
(5)②中发生反应的离子方程式为()。
A.象形图中去掉火焰象形图
B.信号词改为“危险”
C.危险说明改为“数量大时自热;可能起火”
D.一般防范说明只保留“使用前请读标签”
A.病原微生物的传染性及其危害程度
B.病原微生物的生物学特性
C.病原微生物的遗传性特性
D.病原微生物的生化反应特性