 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
铜氨液吸收一氧化碳的反应式是Cu(NH3)2Ac+CO+NH3==Cu[(NH3)CO3]Ac,从该反应特点和化学平衡讨论可知,()、()、增加铜氨液中()、()的浓度,均有利于一氧化碳吸收反应向右进行。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“铜氨液吸收一氧化碳的反应式是Cu(NH3)2Ac+CO+NH…”相关的问题
更多“铜氨液吸收一氧化碳的反应式是Cu(NH3)2Ac+CO+NH…”相关的问题
氮化镓(GaN)是第三代半导体材料,具有热导率高、化学稳定性好等性质,在光电领域和高频微波器件应用等方面有广阔的前景。
(1)传统的氮化镓制各方法是采用GaC13与NH3在一定条件下反应。NH3的电子式为()。
(2)Johnson等人首次在1100℃下用液态镓与氨气制得氮化镓固体,该可逆反应每生成1molH2放出10.3kJ热量。其热化学方程式为()。
(3)在恒容密闭容器中,加入一定量的液态镓与氨气发生上述反应,测得反应平衡体系中NH3的体积分数与压强(p)、温度(T)的关系如图所示。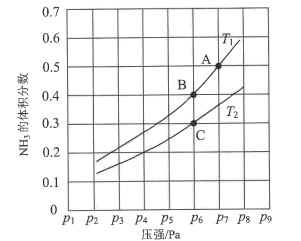 ①下列说法正确的是()(填标号)。
①下列说法正确的是()(填标号)。
a.温度:T1>T2
b.当百分含量ω(NH3)=ω(H2)时,说明该反应处于化学平衡状态
c.A点的反应速率小于C点的反应速率
d.温度恒定为T2,达平衡后再充入氦气(氦气不参与反应),NH3的转化率不变
②既能提高反应速率又能使平衡正向移动的措施有()(写出一条即可)。
③气体分压(p分)=气体总压(p总)×体积分数,用平衡分压代替物质的量浓度也可以表示平衡常数(记作Kp)。在T2时,用含p6的计算式表示C点的()。
(4)如图可表示氮化镓与铜组装成的人工光合系统的工作原理。H+向()(填“左”或“右”)池移动;铜电极上发生反应的电极反应式为()。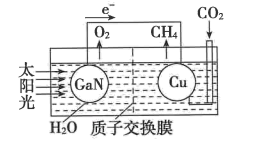
A.促进胃肠运动,排毒增力
B.乳果糖呈酸性,增加氨排出
C.使肠内呈酸性,减少氨的形成和吸收
D.乳果糖与NH3结合
E.分解为乳糖、果糖、氨生成减少
A.Cu(H2O)42+会是较强的酸
B.乙二胺置换H2O会比置换NH3快
C.Cu(H2O)42+的离解常数小
D.Cu(H2O)42+的离解常数大
A.K2[PtCl2(OH)2(NH3)2]
B.[Cu(en)2]Cl2
C.K2[CoCl(NH3)(en)2]
D.[FeY]-(Y为EDTA)
一起氨泄漏事故分析事故经过
2004年6月15日11时40分左右,该化工厂合成车间加氨阀填料压盖破裂,有少量的液氨滴漏。维修工徐某遵照车间指令,对加氨阀门进行填料更换。徐某没敢大意,首先找来操作工,关闭了加氨阀门前后两道阀门;并牵来一根水管浇在阀门填料上,稀释和吸收氨味,消除氨液释放出的氨雾;又从厂安全室借来一套防化服和一套过滤式防防毒面具,佩戴整齐后即投入阀门检修。当他卸掉阀门压盖时,阀门填料跟着冲了出来,瞬间一股液氨猛然喷出,并释放出大片氨雾,包围了整个检修作业点,临近的甲醇岗位和铜洗岗位也笼罩在浓烈的氨味中,情况十分紧急危险。临近岗位的操作人员和安全环保部的安全员发现险情后,纷纷从各处提前消防、防护器材赶来。有的接通了消防水带打开了消火栓,大量喷水压制和稀释氨雾;有时穿上防化服,戴好防毒面具,冲进氨雾中协助险处理。闻讯后赶到的厂领导协助车间指挥,生产调度抓紧指挥操作人员减量调整生产负荷,关闭远距离的相关阀门,停止系统加氨,事故很快得到有效控制和妥善处理,并快速更换了阀门填料,堵住了漏点。一起因严重氨泄漏而即将发生的中毒、着火、有可能爆炸的重特大事故避免了。