 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在制备三苯甲醇的实验中,格氏反应所用溶剂通常为()。这一方面是因为(),可借()排开大部分空气,减少()的接触;另一方面是()可与格氏试剂配位络合,以()的形式溶于()。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在制备三苯甲醇的实验中,格氏反应所用溶剂通常为()。这一方面…”相关的问题
更多“在制备三苯甲醇的实验中,格氏反应所用溶剂通常为()。这一方面…”相关的问题
A.原料不纯或未反应完全的原料造成
B.合成过程中产生的中间体或副产物未完全分离
C.制备过程中加入的溶剂残留造成
D.所用金属器皿及装置等引入杂质
E.长期接触外界条件如光照等引起药物降解造成
十二水合硫酸铝钾[KAI(SO4)2・12H2O]俗名明矾,在生活、医药、工业上应用广泛。下面是实脸室探究从铝土矿(主要成分是氧化铝,含少量氧化铁和二氧化硅杂质)制备明矾的流程示意图。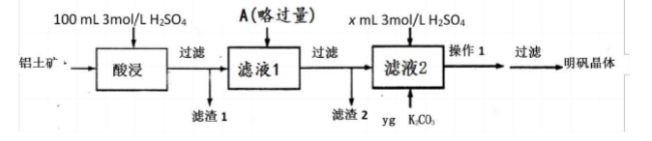 已知:二氧化硅不溶于水,也不与硫酸反应。
已知:二氧化硅不溶于水,也不与硫酸反应。
(1)铝元素在地壳中以()态存在,写出KAl(SO4)·12H2O溶于水的电离方程式()。当明矾溶液中混有NaCl时,简述如何检验Cl()。
(2)滤渣1主要为()(填化学式);以Al2O3为原料,制备该单质铝的反应方程式()。
(3)若A为金属单质,则滤渣2的成分有()。
(4)操作1是蒸发溶剂至有大量晶膜、冷却结晶。实验室进行该操作时,需要的实验仪器有铁架台、()。
(5)如图为某硫酸试剂瓶的标签。若用其配制100mL3mol/L的溶液,需该硫酸()mL(含ρ的表达式)。若此硫酸物质的量浓度为c1,35%的硫酸物质的浓度为c2,则c1()2c2(填大于,小于或等于)。 (6)工业生产中,获取明矾晶体后的母液应该()(填序号)。
(6)工业生产中,获取明矾晶体后的母液应该()(填序号)。
A、弃去
B、返回酸浸流程重复利用
C、返回滤液1重复利用
D、返回滤液2重复利用
聚合氯化铝是一种新型、高效絮凝剂和净水剂,其单体是液态的碱式氯化铝(Al2(OH)nCl6-n)。本实验采用铝盐溶液水解絮凝法制备碱式氯化铝。其制备原料为分布广、价格廉的高岭土,化学组成为:Al2O3(25%~34%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)以及少量杂质和水分。已知氧化铝有多种不同的结构,化学性质也有差异,且一定条件下可相互转化;高岭土中的氧化铝难溶于酸。制备碱式氯化铝的实验流程如下
 根据流程图答复以下问题:
根据流程图答复以下问题:
问题一、“煅烧”的目的是()。
问题二、配制质量分数15%的盐酸需要200mL30%的浓盐酸(密度约为1.15g·cm-3)和()g蒸馏水,配制用到的仪器有烧杯、玻璃棒、()。
问题三、“溶解”过程中发生反应的离子方程式为()。
问题四、加少量铝粉的主要作用是()。
问题五、“调节溶液pH在~4.5”的过程中,除添加必要的试剂,还需借助的实验用品是();“蒸发浓缩”需保持温度在90~100℃,控制温度的实验方法是()。
在一定条件下发生的下列反应中,属于消去反应的是()。
A.乙醇和氢溴酸反应生成溴乙烷
B.苯和浓硝酸反应生成硝基苯
C.乙酸和乙醇反应生成乙酸乙酯
D.由乙醇制备乙烯
固体化合物X由四种常见的元素组成,为探究其成分,某学生进行如下实验: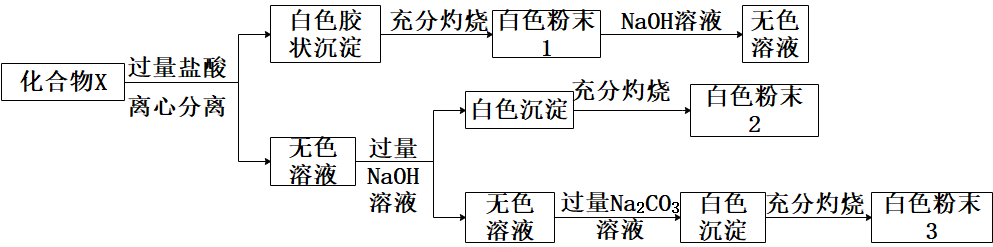 ①20.8gX固体进行实验,得到白色粉末1质量12.0g,白色粉末2质量为6.0g;
①20.8gX固体进行实验,得到白色粉末1质量12.0g,白色粉末2质量为6.0g;
②白色粉末2可用作耐高温材料,白色粉末3是一种常见干燥剂;请回答问题:
(1)X中金属元素的名称是()。
(2)化合物X与足量盐酸反应离子方程式()。
(3)在高温条件下,白色粉末2中某元素单质与白色粉末1反应,是工业制备另一种单质方法之一,写出该反应的化学方程式()。