 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
计算用0.100mol·L-1HC1溶液滴定0.050mol·L-1Na2B4O7溶液至计量点时
的pH选用何种指示剂?
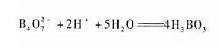
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“计算用0.100mol·L-1HC1溶液滴定0.050mol…”相关的问题
更多“计算用0.100mol·L-1HC1溶液滴定0.050mol…”相关的问题
A.5.66
B.4.66
C.3.66
D.2.66
用0.1000mol/LHCl溶液滴定0.1000mol/LNa2CO3溶液至pH5.00。计算有百分之几的Na2CO3变成了H2CO3?剩下的主要组分是什么?如果煮沸溶液以除尽CO2,冷却后溶液的pH为多少?(H2CO3的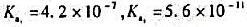 )
)
A.配制过程中要求加热至95℃~100℃
B.用蒸馏水溶解硫酸钠
C.10水硫酸钠和无水硫酸钠用量一样
D.溶液在室温状态下静置24h后测相对密度
E.通过蒸馏水和硫酸钠用量,采用理论计算的方法计算溶液相对密度
电池: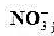 选择性电极[
选择性电极[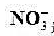 (a=5.0X10-3mo1/L)]ISCE的电动势为0.386V。计算:
(a=5.0X10-3mo1/L)]ISCE的电动势为0.386V。计算:
(1)用未知活度的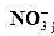 溶液代替已知活度的
溶液代替已知活度的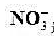 溶液,测得其电动势为0.429v,未知溶液中
溶液,测得其电动势为0.429v,未知溶液中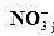 活度为多少?
活度为多少?
(2)若液接电位产生的误差为士0.002V,活度在什么范围内变化?