题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列热化学方程式书写正确的是()。
A.Fe+S=FeS△H=-95.6kJ/mol(反应热)
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=+57.3kJ/mol(中和热)
C.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g)△H=-1367.0kJ/mol(燃烧热)
D.S(s)+O2(g)=SO2(g)△H=-269.8kJ/mol(反应热)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.Fe+S=FeS△H=-95.6kJ/mol(反应热)
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=+57.3kJ/mol(中和热)
C.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g)△H=-1367.0kJ/mol(燃烧热)
D.S(s)+O2(g)=SO2(g)△H=-269.8kJ/mol(反应热)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列热化学方程式书写正确的是()。”相关的问题
更多“下列热化学方程式书写正确的是()。”相关的问题
298.15K时,已知下列热化学方程式
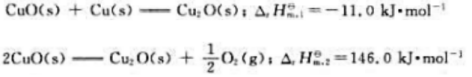
则298.15K时,CuO(s)的标准摩尔生成焓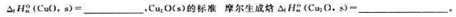
A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多
B.从C(石墨)=C(金刚石)△H=+1.9kJ•mol-1,可知石墨比金刚石更稳定
C.2gH2完全燃烧生成液态水放出285.8kJ热量,则氢气燃烧的热化学方程式为2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ•mol-1
D.由H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ•mol-1,可知:含1molCH3COOH的溶液与含1molNaOH的溶液混合,放出热量等于57.3kJ
A.CO2通入NaAlO2溶液中AlO+CO2+H2O===Al(OH)3↓+CO
B.Al2O3与过量氨水Al2O3+6NH3•H2O===2Al3++6NH
C.向AlCl3溶液中加入过量NaOH溶液Al3++3OH-===Al(OH)3↓
D.向AlCl3溶液中滴入过量的氨水Al3++3NH3•H2O===Al(OH)3↓+3NH
以下离子方程式书写正确的选项是()。
A.烧碱溶液与小苏打溶液反响:OH-+HCO3-H2O+CO2↑
B.铝粉与烧碱溶液反响:2Al+2OH-+H2O2AlO2-+2H2↑
C.氯化亚铁溶液中滴加氯水:2Fe2++Cl22Fe3++2Cl-
D.氯气通入冷的氢氧化钠溶液中:2Cl2+2OH-3Cl-+ClO-+H2O
某氮肥厂氨氮废水中的氮元素多以NH和NH3·H2O的形式存在,该废水的处理流程如下:![]()
问题一、过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30℃,通空气将氨赶出并回收。
①用离子方程式表示加NaOH溶液的作用:()。
②用化学平衡原理解释通空气的目的:()。
问题二、过程Ⅱ:在微生物作用的条件下,NH经过两步反应被氧化成NO。两步反应的能量变化示意图如下:
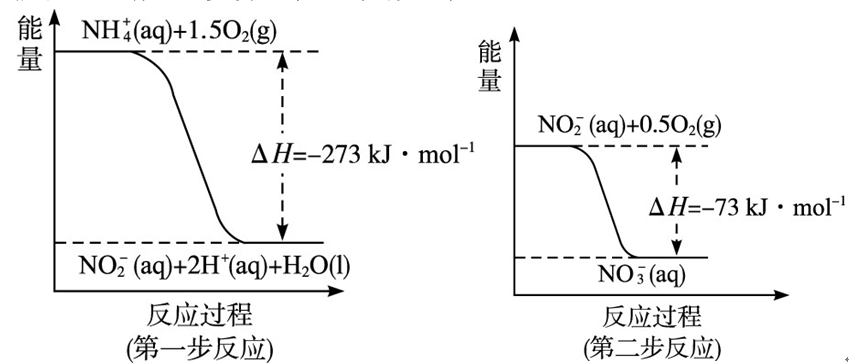
①第一步反应是()反应(选填“放热”或“吸热”),判断依据是()。
②1molNH(aq)全部氧化成NO(aq)的热化学方程式是()。
问题三、过程Ⅲ:一定条件下,向废水中加入CH3OH,将HNO3复原成N2。假设该反应消耗32gCH3OH转移6mol电子,则参加反应的复原剂和氧化剂的物质的量之比是()。
过度排放CO2会造成”温室效应“,科学家正在研究如何将CO2转化为可以利用的资源,其中一种方案就是将CO2转化为可再生燃料甲醇(CH3OH)。其化学方程式为: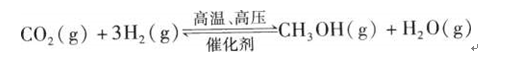
请填空:
问题一、写出上述反应的平衡常数表达式K=()。
问题二、在容积为2L的密闭容器中,用一定量二氧化碳与一定量氢气在一定条件下合成甲醇,实验结果如下图。以下说法正确的选项是()。
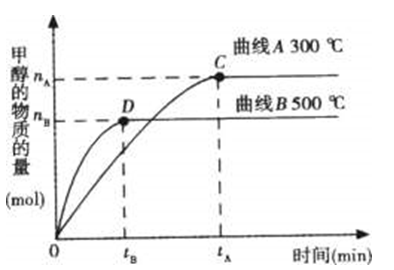
A在300℃,从反应开始到平衡,甲醇的平均反应速率
B反应体系从300℃升温到500℃,平衡常数K变大
C该反应的正反应为放热反应
D处于C点的反应体系从300℃升温到500℃n(H2)/n(CH3OH)增大
问题三、25℃、1.01×105Pa时16g液态甲醇完全燃烧,当恢复至原状态时,放出362.9kJ热量,此反应的热化学方程式为()。
问题四、选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此燃料电池负极应加入或通入的物质是,正极的电极反应式为()。
最近科学家提出“绿色自由”设想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇。“绿色自由”设想技术流程如下
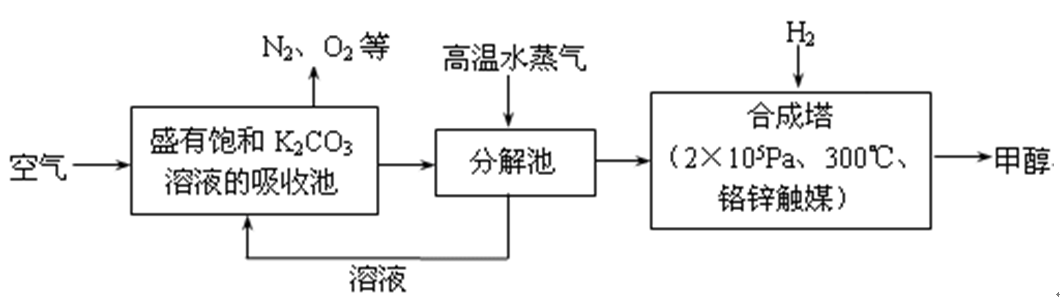
问题一、分解池中发生分解反应的物质是()。
问题二、在合成塔中,假设有CO2与足量H2kJ的热量,试写出合成塔中发生反应的热化学方程式()
问题三、①从平衡移动原理分析,低温有利于原料气的转化,而实际生产中采用300℃的温度,原因之一是考虑到催化剂的催化活性,原因之二是()。
②“绿色自由”设想技术流程中常包括物质和能量的“循环利用”,上述流程中能表达“循环利用”的除碳酸钾溶液外,还包括()。
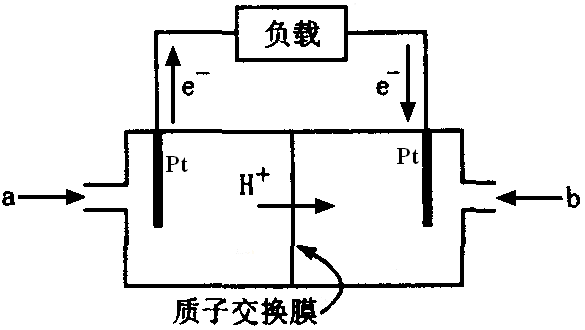
问题四、右图是甲醇燃料电池的结构示意图。已知电池总反应为:2CH3OH+3O2=2CO2+4H2O。通入a一端的电极是(填“正极”或“负极”),负极发生的电极反应是()。
 答案:
答案:
氮化镓(GaN)是第三代半导体材料,具有热导率高、化学稳定性好等性质,在光电领域和高频微波器件应用等方面有广阔的前景。
(1)传统的氮化镓制各方法是采用GaC13与NH3在一定条件下反应。NH3的电子式为()。
(2)Johnson等人首次在1100℃下用液态镓与氨气制得氮化镓固体,该可逆反应每生成1molH2放出10.3kJ热量。其热化学方程式为()。
(3)在恒容密闭容器中,加入一定量的液态镓与氨气发生上述反应,测得反应平衡体系中NH3的体积分数与压强(p)、温度(T)的关系如图所示。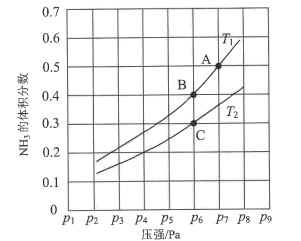 ①下列说法正确的是()(填标号)。
①下列说法正确的是()(填标号)。
a.温度:T1>T2
b.当百分含量ω(NH3)=ω(H2)时,说明该反应处于化学平衡状态
c.A点的反应速率小于C点的反应速率
d.温度恒定为T2,达平衡后再充入氦气(氦气不参与反应),NH3的转化率不变
②既能提高反应速率又能使平衡正向移动的措施有()(写出一条即可)。
③气体分压(p分)=气体总压(p总)×体积分数,用平衡分压代替物质的量浓度也可以表示平衡常数(记作Kp)。在T2时,用含p6的计算式表示C点的()。
(4)如图可表示氮化镓与铜组装成的人工光合系统的工作原理。H+向()(填“左”或“右”)池移动;铜电极上发生反应的电极反应式为()。