 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知电对Cl2/Cl-,Br2/Br-,I2/I-的 分别为1.36V,1.07V,0.54V。今有一种Cl-,Br-,I-的混合溶液,标准状态时能氧化I-而不氧化Br-和Cl-的物质是( )
分别为1.36V,1.07V,0.54V。今有一种Cl-,Br-,I-的混合溶液,标准状态时能氧化I-而不氧化Br-和Cl-的物质是( )
A.KMnO4(
B.MnO2(
C.Fe2(SO4)3(
D.CuSO4(
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 分别为1.36V,1.07V,0.54V。今有一种Cl-,Br-,I-的混合溶液,标准状态时能氧化I-而不氧化Br-和Cl-的物质是( )
分别为1.36V,1.07V,0.54V。今有一种Cl-,Br-,I-的混合溶液,标准状态时能氧化I-而不氧化Br-和Cl-的物质是( )A.KMnO4(
B.MnO2(
C.Fe2(SO4)3(
D.CuSO4(
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知电对Cl2/Cl-,Br2/Br-,I2/I-的分别为1…”相关的问题
更多“已知电对Cl2/Cl-,Br2/Br-,I2/I-的分别为1…”相关的问题
A..Cl->Br->I-
B.Cl->I->Br-
C.Br->I->Cl-
D.I->Br->Cl-
A.2、Cl2、Br2、I2的氧化性逐渐减弱
B.HF、HCl、HBr、HI的热稳定性逐渐减弱
C.-、Cl-、Br-、I-的还原性逐渐增强
D.卤素单质按F2、Cl2、Br2、I2的顺序颜色逐渐变浅,密度逐渐增大
A.卤素离子的还原性:F-<Cl-<Br-<I-
B.酸性:HIO4<HBrO4<HClO4
C.单质与氢气化合由难到易顺序:F2<Cl2<Br2<I2
D.氢卤酸的酸性:HF>HCl>HBr>HI
含有Cl-和Br-的混合溶液,欲使Br-氧化为Br2而不使Cl-氧化,应选择()
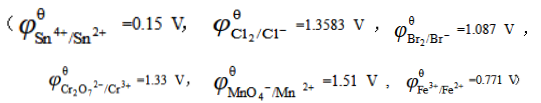
A.SnCl4
B.K2Cr2O7
C.KMnO4
D.Fe3+
A.Fe2+;
B.Cu
C.Mg
D.Cl-
已知Eθ(MnO-4/Mn2+)=1.51V,Eθ(Cl2/Cl-)=1.36V,若将此两电对组成原电池,请写出:
(1)该电池的电池符号;
(2)写出正负电极的电极反应和电池反应以及电池标准电动势;
(3)计算电池反应在25℃时和Kθ;
(4)当[H+] = 1.0×10-2mol•L-1,而其他离子浓度均为1.0 mol•L-1,= 100 kPa时的电池电动势.
A.I2能氧化Fe2+
B.Fe3+能氧化Br-
C.I2能氧化Br-
D.Br2能氧化Fe2+
A.Cl-、Br-、CrO42-
B.Br-、Cl-、CrO42-
C.CrO42-、Cl-、Br-
D.三者同时沉淀
烯烃对于亲电试剂(如:Br2,Cl2,HCl)的加成比炔烃是更加活泼的,而当炔烃和这些相同的亲电试剂作用时却容易停止加成反应在“烯的阶段”。这是否有矛盾,请给予解释。