 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知Eθ(Fe3+/Fe2+)=0.77 V,Eθ(Cl2/Cl-)=1.36 V,问:当c(Cl-)= 0.010 mol.L-1,c(Fe2+)=0.10 m
已知Eθ(Fe3+/Fe2+)=0.77 V,Eθ(Cl2/Cl-)=1.36 V,问:当c(Cl-)= 0.010 mol.L-1,c(Fe2+)=0.10 mol.-1,(其余物种处于标准态下),分别计算 Eθ(Fe3+/Fe2+)和Eθ(Cl2/Cl-)的值,并判断反应
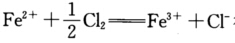 往哪个方向进行?
往哪个方向进行?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“已知Eθ(Fe3+/Fe2+)=0.77 V,Eθ(Cl2/…”相关的问题
更多“已知Eθ(Fe3+/Fe2+)=0.77 V,Eθ(Cl2/…”相关的问题
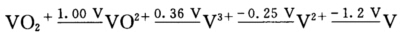 并已知:Eθ(Fe3+/Fe2+)=+0.77 V;Eθ(Zn2+/Zn)=一0.76 V Eθ(Sn2+/Sn)=一0.14 V;Eθ(O2/H2O)=+1.229 V (1)Eθ(VO2+/V2+)________________________________; (2)欲使VO2+→V3+,可选用还原剂________________________________; (3)欲使VO2+→V3+,可选用还原剂________________________________; (4)钒在空气中稳定的形态有________________________________。
并已知:Eθ(Fe3+/Fe2+)=+0.77 V;Eθ(Zn2+/Zn)=一0.76 V Eθ(Sn2+/Sn)=一0.14 V;Eθ(O2/H2O)=+1.229 V (1)Eθ(VO2+/V2+)________________________________; (2)欲使VO2+→V3+,可选用还原剂________________________________; (3)欲使VO2+→V3+,可选用还原剂________________________________; (4)钒在空气中稳定的形态有________________________________。
















