 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
1mol理想气体在300K下,分别经过下列三种过程从50dm3膨胀到100dm3,计算以下各过程的Q,W,△U,△H和△S。 (1)可
1mol理想气体在300K下,从始态100KPa到下列各过程,计算以下各过程的Q,W,△U,△H和△S。
(1)可逆膨胀到压力50Kpa;
(2)反抗恒定外压50Kpa,不可逆膨胀到平衡状态;
(3)向真空膨胀到原体积的2倍。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
1mol理想气体在300K下,从始态100KPa到下列各过程,计算以下各过程的Q,W,△U,△H和△S。
(1)可逆膨胀到压力50Kpa;
(2)反抗恒定外压50Kpa,不可逆膨胀到平衡状态;
(3)向真空膨胀到原体积的2倍。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“1mol理想气体在300K下,分别经过下列三种过程从50dm…”相关的问题
更多“1mol理想气体在300K下,分别经过下列三种过程从50dm…”相关的问题
1mol理想气体在298K、101.3kPa下等温可逆膨胀,若过程的△G=-2983J,则终态的压力为多少
始态为T1=300K,P1=200kPa的某双原子理想气体1mol,经两条不同途径变化到T2=300K,P2=100kPa的末态。求各步的Q、△S。

A.向左进行
B.向右进行
C.处于平衡状态
D.无法确定
一理想气体开始处于T1=300K,p1=3.039×105Pa,V1=4m3。该气体等温地膨胀到体积为16m3,接着经过一等体过程而达到某一压强,从这个压强再经一绝热压缩就能使气体回到它的初态。设全部过程都是可逆的。
已知氮(N2,g)的摩尔定压热容与温度的两数关系为
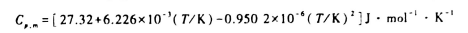
将始态为300K,100kPa下的1molN2(g)置于1000K的热源中,求系统分别经(1)恒压过程;(2)恒容过程达到平衡态时的Q,ΔS及ΔSm.