 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某实验室废水含有较多的盐酸,排放前应加入某种试剂将废水调至中性,下列试剂中最合适的是()
A.KNO3溶液
B.gNO3溶液
C.NaOH溶液
D.稀醋酸
 答案
答案
C、NaOH溶液
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.KNO3溶液
B.gNO3溶液
C.NaOH溶液
D.稀醋酸
 答案
答案
C、NaOH溶液
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某实验室废水含有较多的盐酸,排放前应加入某种试剂将废水调至中…”相关的问题
更多“某实验室废水含有较多的盐酸,排放前应加入某种试剂将废水调至中…”相关的问题
A.加入用HNO3酸化的Ba(NO3)2溶液
B.用HNO3酸化,再加Ba(NO3)2溶液
C.先用盐酸酸化,再加BaCl2溶液
D.直接加入盐酸酸化的BaCl2溶液
以下各项均是某工厂为防止排出不符合排放标准的废水的控制系统的组成部分,除了
A.在排放前,对许可证中所指明的废水成分进行化学分析。
B.通过政策.培训和建议标牌)详细说明哪些物质可以经工厂内的污水槽和地面排水管处理。
C.定期用大量净水冲洗污水槽和地面排水管,以确保污染物质被充分地稀释。
D.为工厂的预处理系统制定一个预防性的维修方案。
除了哪项,以下各项均是某工厂为防止排出不符合排放标准的废水的控制系统的组成部分:
A.在排放前,对许可证中所指明的废水万分进行化学分析。
B.(通过政策、培训和建议标牌)详细说明哪些物质可以经工厂内的污水槽和地面排水管处理。
C.为工厂的预处理系统制定一个预防性的维修方案。
D.定期由大量净水冲洗污水槽和地面排水管,以确保污染物质被充分地稀释。
A.SO2的水溶液能导电说明SO2是电解质
B.HClO是弱酸,所以NaClO是弱电解质
C.某无色溶液加入NaOH溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,则该溶液含有NH4+
D.某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液一定存在大量CO32-
A.向未知溶液中加入AgNO3溶液,有白色沉淀产生
B.向未知溶液中加入AgNO3溶液,有白色沉淀产生,加入盐酸,沉淀不消失
C.向未知溶液中加入稀硝酸酸化后,再加入AgNO3溶液,有白色沉淀产生
D.向未知溶液中加入稀盐酸酸化后,再加入AgNO3溶液,有白色沉淀产生
A.禁止向海域排放油类、酸液、碱液、剧毒废液和高、中水平放射性废水
B.严格限制向海域排放低水平放射性废水;确需排放的,必须严格执行国家水污染物排放标准的规定
C.禁止向海域排放含有不易降解的有机物和重金属的废水
D.含有机物和营养物质的工业废水、生活污水,不得向海湾、半封闭海及其他自净能力较差的海域排放
A.Q1·C0
B.(Q1+Q0)·C0
C.(Q1+Q0-ΔQ)·C0
D.(Q1-ΔQ)·C0
A.特别法优于一般法
B.后法优于前法
C.前法优于后法
D.一般法优于特别法
随着工业的迅速发展,产生的废水对水体的污染也日趋严重。通过控制溶液的pH对工业废水中的金属离子进行别离是实际工作中经常使用的方法。下表是常温下金属氢氧化物的Ksp(沉淀溶解平衡常数)和金属离子在某浓度下开始沉淀所需的pH(表中浓度为相应pH时溶液中有关金属离子产生沉淀的最小浓度;当溶液中金属离子浓度小于10-5mol•L-1时通常认为该离子沉淀完全)。 问题一、某厂排出的废水中含有Cu2+和Fe3+,测得其浓度均小于0.1mol•L-l。为除去其中的Fe3+,回收铜,需控制的pH范围是()。
问题一、某厂排出的废水中含有Cu2+和Fe3+,测得其浓度均小于0.1mol•L-l。为除去其中的Fe3+,回收铜,需控制的pH范围是()。
问题二、为了处理含有Cr2O72-酸性溶液的工业废水,采用如下方法:向废水中加人适量NaCl,以Fe为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成排出,从而使废水中铬含量低于排放标准
①Cr2O72-转变为Cr3+的离子方程式为()。
②pH对废水中Cr2072-去除率的影响如右图。你认为电解过程中溶液的pH取值在()范围内对降低废水中的铬含量最有利,请说明理由:()。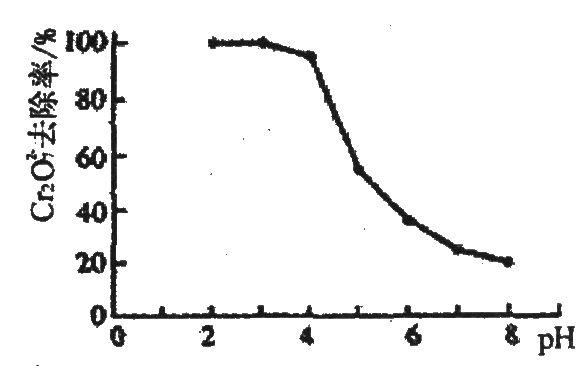
问题三、沉淀转化在生产中也有重要应用。例如,用Na2C03溶液可以将锅炉水垢中的CaS04转化为较疏松而易清除的CaC03,该沉淀转化到达平衡时,其平衡常数K=()。(已知Ksp(CaS04)=9.1x10-6,Ksp(CaC03)=2.8x10-9)