 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
阳极用镍、阴极用铁电解NiSO4,主要电解产物为()。A.阳极Ni溶解,阴极Ni析出B.阳极有O2产生C.阴极产
阳极用镍、阴极用铁电解NiSO4,主要电解产物为()。
A.阳极Ni溶解,阴极Ni析出
B.阳极有O2产生
C.阴极产生Ni和H2
D.阴极有H2产生
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
阳极用镍、阴极用铁电解NiSO4,主要电解产物为()。
A.阳极Ni溶解,阴极Ni析出
B.阳极有O2产生
C.阴极产生Ni和H2
D.阴极有H2产生
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“阳极用镍、阴极用铁电解NiSO4,主要电解产物为()。A.阳…”相关的问题
更多“阳极用镍、阴极用铁电解NiSO4,主要电解产物为()。A.阳…”相关的问题
用金属铜作电极,电解稀CuSO4水溶液,开始一段时间阴阳极区溶液颜色的变化是()。
A.阳极区变深、阴极区变浅
B.阳极区变浅、阴极区变深
C.阴阳极区都变深
D.阴阳极区都变浅
A.比氢更负电性金属
B.具有电子导电能力和不被氧化的石墨(碳)
C.电位在电解条件下,位于水的稳定状态图中氧线以上的各种金属,其中首先是铂
D.在电解条件下发生钝化的各种金属,如硫酸溶液中的铅;碱性溶液中的镍和铁
A.待加工铝质工件为阳极
B.可选用不锈钢网作为阴极
C.阴极的电极反应式为
D.硫酸根离子在电解过程中向阳极移动
电解工作原理的实际应用非常广泛。
(1)请画出铜棒镀银的简易装置设计图()。(实验可选用品:铜棒,银片,石墨棒,硫酸铜溶液,硝酸银溶液,导线,电源,烧杯)。
(2)工业上为了处理含有Cr2O12-的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是()(填字母)。
A、阳极反应:Fe-2e-=Fe2+
B、阴极反应:2H++2e-=H2↑
C、在电解过程中工业废水由酸性变为碱性
D、可以将铁电极改为石墨电极
(3)某同学设计了如图装置进行以下电化学实验。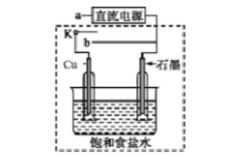 ①当开关K与a连接时,两极均有气泡产生,则阴极为()电极。
①当开关K与a连接时,两极均有气泡产生,则阴极为()电极。
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为()。请写出此时Cu电极上的电极反应()。
(4)某溶液中含有的离子如下表: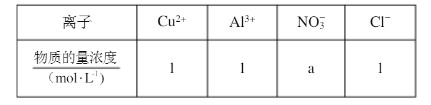 用惰性电极电解该溶液,当电路中有3mole-通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),下列说法正确的是()(填字母)。
用惰性电极电解该溶液,当电路中有3mole-通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),下列说法正确的是()(填字母)。
A、电解后溶液呈酸性
B、a=3
C、阳极生成1.5molCl2
D、阴极析出的金属是铜与铝
A.阴阳两极都用石墨
B.铜作阳极铁作阴极
C.铁作阳极铜作阴极
D.铜作阳极铂作阴极