 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
在1mol·L-1HC1溶液中用Fe3+溶液滴定Sn2+时,计算:(1)此氧化还原反应的平衡常数及化学计量点时反应进行的程度:滴定时电位突跃范围.在此滴定中应选用什么指示剂?用所选指示剂时,滴定终点是否和化学计量点一致?
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在1mol·L-1HC1溶液中用Fe3+溶液滴定Sn2+时,…”相关的问题
更多“在1mol·L-1HC1溶液中用Fe3+溶液滴定Sn2+时,…”相关的问题
下列体系电位滴定至化学计量点时的电池电动势(用SCE作负极)为多少?
(a)在1mol·L-1HCL介质中,用Ce4+滴定Sn2+;
(b)在1mol·L-1H2SO4介质中,用Fe3+滴定UIV;
(c)在lmol·L-1H2SO4介质中,用Ce4+滴定vo2+.
A.Fe3+>Mg2+>Na+>K+>H+
B.Fe3+>Na+>H+>Mg2+>K+
C.H+>K+>Na+>Mg2+>Fe3+
D.Fe3+>Mg2+>K+>Na+>H+
298K时,在Fe3+,Fe2+的混合溶液中加入NaOH时,有Fe(OH)3和Fe(OH)2沉淀生成(假如没有其它反应发生)。当沉淀反应达到平衡时,保持c(OH-)=1.0molL-1,计算

放出H2(105Pa),利用
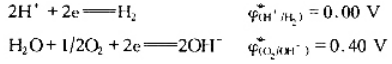
计算理论分解电压,实际分解电压将比理论值大还是小?为什么?若0.10mol·dm-3的NaOH代替硫酸,分解电压为多少?
A.5.66
B.4.66
C.3.66
D.2.66