 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知氮(N2,g)的摩尔定压热容与温度的两数关系为将始态为300K,100kPa下的1molN2(g)置于
已知氮(N2,g)的摩尔定压热容与温度的两数关系为
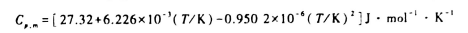
将始态为300K,100kPa下的1molN2(g)置于1000K的热源中,求系统分别经(1)恒压过程;(2)恒容过程达到平衡态时的Q,ΔS及ΔSm.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知氮(N2,g)的摩尔定压热容与温度的两数关系为
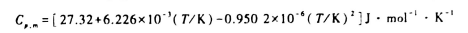
将始态为300K,100kPa下的1molN2(g)置于1000K的热源中,求系统分别经(1)恒压过程;(2)恒容过程达到平衡态时的Q,ΔS及ΔSm.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知氮(N2,g)的摩尔定压热容与温度的两数关系为将始态为3…”相关的问题
更多“已知氮(N2,g)的摩尔定压热容与温度的两数关系为将始态为3…”相关的问题
已知CH3COOH(g),CH4(g)和CO2(g)的平均摩尔定压热容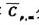 分别为52.3J·mol-1·K-1,37.7J·mol-1·K-1和31.4J·mol-1·K-1.试由教材附录中三化合物的标准摩尔生成焓计算1000K时下列反应的
分别为52.3J·mol-1·K-1,37.7J·mol-1·K-1和31.4J·mol-1·K-1.试由教材附录中三化合物的标准摩尔生成焓计算1000K时下列反应的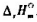 .
.
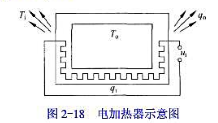
现将隔板撤掉,整个系统达到热平衡,求末态温度t及过程的ΔH.已知:Ar(g)和Cu(s)的摩尔定压热容Cp·m分别为20.786J·mol-1·K-1及24.435J·mol-1·K-1,且假设均不随温度而变。
冰(H2O,s)在100kPa下的熔点为0℃,此条件下的摩尔融化焓 =6.012kJ·mol-1.已知在-10~0℃范围内过冷水(H2O,l)和冰的摩尔定压热容分别为76.28J·mol-1·K-1和37.20J·mol-1·
=6.012kJ·mol-1.已知在-10~0℃范围内过冷水(H2O,l)和冰的摩尔定压热容分别为76.28J·mol-1·K-1和37.20J·mol-1·
K-1.求在常压及-10℃下过冷水结冰的摩尔凝固焓.
生成焓;(2)N2H4的标准摩尔燃烧焓;(3)N2H4与N2O4反应生成N2(g)和H2O(I)的标准摩尔反应焓.已知:
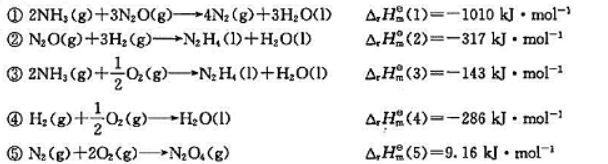
A.升高温度使吉布斯自由能变和和标准吉布斯自由能变均增大
B.升高温度可以使平衡向右移动
C.升高温度可以使平衡常数增大
D.正反应自发时,随着反应进行,N2和H2分压逐渐减小,NH3分压逐渐增大,所以平衡常数Kp逐渐增大
用BET法测量某种硅胶的比表面积。在-195℃、不同N2分压下,硅胶的N2平衡吸附量如下:
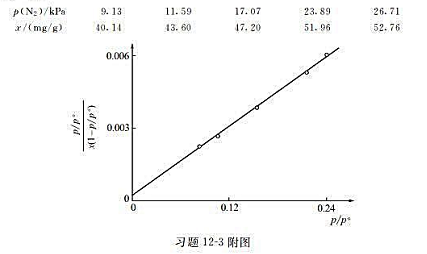
已知—195℃时N2的饱和蒸气压为111.0kPa,每个氮分子的截面积AD为0.154mm2,试求这种硅胶的比表面积。
已知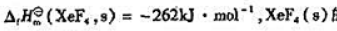 的升华焓为47kJ·mol-1,F2(g)的键解离能为158kJ·mol-1.计算:
的升华焓为47kJ·mol-1,F2(g)的键解离能为158kJ·mol-1.计算:
(1)XeF4(g)的标准摩尔生成焓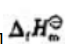 (XeF4,g);
(XeF4,g);
(2)XeF4分子中Xc-F键的键能.